- Mô tả
- Chỉ định
- Dược lực học
- Động lực học
- Tương tác thuốc
- Chống chỉ định
- Liều lượng & cách dùng
- Tác dụng phụ
- Lưu ý
- Quá liều
- Mô tả
- Chỉ định
- Dược lực học
- Động lực học
- Tương tác thuốc
- Chống chỉ định
- Liều lượng & cách dùng
- Tác dụng phụ
- Lưu ý
- Quá liều
Lorlatinib: Thuốc điều trị ung thư phổi nhắm trúng đích ALK và ROS1
02/04/2026
Mặc định
Lớn hơn
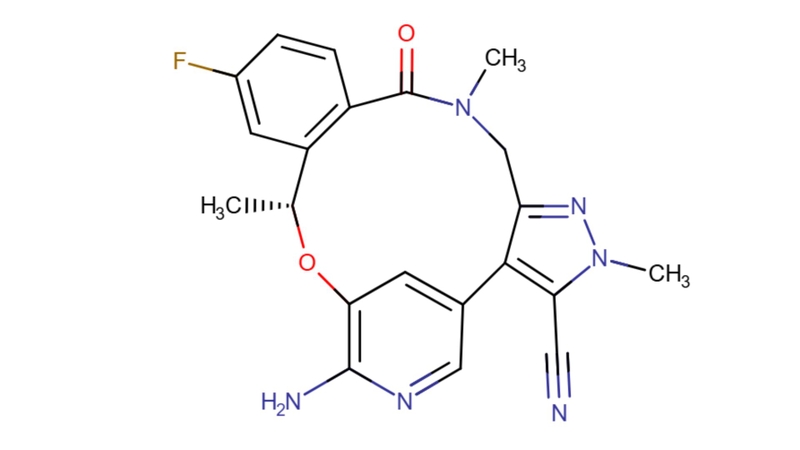
Lorlatinib là một thuốc điều trị ung thư thuộc nhóm ức chế tyrosine kinase, được sử dụng chủ yếu trong điều trị ung thư phổi không tế bào nhỏ có đột biến gen ALK hoặc ROS1. Hoạt chất này được thiết kế để vượt qua hàng rào máu não, giúp kiểm soát cả các di căn não thường gặp ở bệnh nhân ung thư phổi tiến triển. Lorlatinib thường được dùng khi bệnh kháng hoặc tiến triển sau các thuốc ức chế ALK thế hệ trước. Thuốc có thể gây một số tác dụng phụ trên thần kinh trung ương và rối loạn lipid máu, vì vậy cần được sử dụng dưới sự theo dõi chặt chẽ của bác sĩ.
- Mô tả
- Chỉ định
- Dược lực học
- Động lực học
- Tương tác thuốc
- Chống chỉ định
- Liều lượng & cách dùng
- Tác dụng phụ
- Lưu ý
- Quá liều
- Mô tả
- Chỉ định
- Dược lực học
- Động lực học
- Tương tác thuốc
- Chống chỉ định
- Liều lượng & cách dùng
- Tác dụng phụ
- Lưu ý
- Quá liều
Mô tả
Tên thuốc gốc (Hoạt chất)
Lorlatinib
Loại thuốc
Thuốc điều trị ung thư.
Dạng thuốc và hàm lượng
Lorlatinib được bào chế chủ yếu dưới dạng viên nén bao phim dùng đường uống. Thuốc hiện có hai hàm lượng phổ biến là 25 mg và 100 mg, giúp bác sĩ linh hoạt điều chỉnh liều trong quá trình điều trị.
Chỉ định
Lorlatinib được chỉ định sử dụng đơn trị liệu cho bệnh nhân trưởng thành mắc ung thư phổi không tế bào nhỏ (NSCLC) giai đoạn tiến triển có đột biến ALK dương tính. Thuốc có thể dùng cho những người chưa từng điều trị bằng thuốc ức chế ALK trước đó, hoặc cho bệnh nhân bệnh tiếp tục tiến triển sau khi đã được điều trị bằng các thuốc ức chế ALK trước đây. Lorlatinib giúp ức chế hoạt động của protein kinase ALK và ROS1 bất thường, từ đó góp phần kiểm soát sự phát triển của tế bào ung thư.
Dược lực học
Lorlatinib là một thuốc ức chế tyrosine kinase có tính chọn lọc cao, hoạt động bằng cách cạnh tranh với adenosine triphosphate (ATP) tại vị trí hoạt động của các kinase ALK (anaplastic lymphoma kinase) và ROS1 (c-ros oncogene 1). Nhờ cơ chế này, thuốc có thể ngăn chặn tín hiệu tăng sinh bất thường của tế bào ung thư.
Trong các nghiên cứu tiền lâm sàng, Lorlatinib cho thấy khả năng ức chế mạnh hoạt tính của ALK dạng bình thường cũng như nhiều biến thể đột biến có ý nghĩa lâm sàng, được đánh giá qua các thử nghiệm sử dụng enzyme tái tổ hợp và mô hình tế bào. Thuốc cũng thể hiện tác dụng chống khối u rõ rệt trên mô hình chuột mang khối u cấy ghép có sự kết hợp giữa protein EML4 (echinoderm microtubule-associated protein-like 4) và các biến thể của ALK, bao gồm các đột biến L1196M, G1269A, G1202R và I1171T. Đáng chú ý, các đột biến như G1202R và I1171T thường liên quan đến tình trạng kháng với một số thuốc ức chế ALK thế hệ trước như Alectinib, Brigatinib, Ceritinib và Crizotinib.
Ngoài ra, Lorlatinib còn có khả năng thấm qua hàng rào máu - não, điều này giúp thuốc phát huy tác dụng trong các mô hình chuột có khối u não cấy ghép EML4-ALK hoặc EML4-ALK L1196M, cho thấy tiềm năng kiểm soát các tổn thương di căn trong hệ thần kinh trung ương.
Động lực học
Hấp thu
Sau khi uống, Lorlatinib được hấp thu khá nhanh vào tuần hoàn. Nồng độ thuốc trong huyết tương thường đạt mức tối đa sau khoảng 1,2 giờ khi dùng liều đơn 100 mg và khoảng 2,0 giờ khi sử dụng lặp lại liều 100 mg mỗi ngày. Sinh khả dụng tuyệt đối trung bình của Lorlatinib khi dùng đường uống đạt khoảng 80,8%.
Ảnh hưởng của thức ăn đối với sự hấp thu của thuốc tương đối nhỏ. Khi dùng Lorlatinib cùng bữa ăn giàu chất béo và năng lượng, nồng độ thuốc trong cơ thể chỉ tăng khoảng 5% so với khi dùng lúc đói, vì vậy thuốc có thể uống cùng hoặc không cùng bữa ăn mà không ảnh hưởng đáng kể đến hiệu quả.
Ở bệnh nhân ung thư dùng Lorlatinib 100 mg mỗi ngày một lần, nồng độ đỉnh trung bình trong huyết tương (Cmax) theo trung bình hình học đạt khoảng 577 ng/mL với hệ số biến thiên (CV) 42%. Diện tích dưới đường cong nồng độ - thời gian trong 24 giờ (AUC₍24₎) trung bình khoảng 5.650 ng·h/mL (CV 39%). Độ thanh thải biểu kiến qua đường uống của thuốc được ước tính khoảng 17,7 L/giờ, phản ánh khả năng đào thải của cơ thể đối với hoạt chất này.
Phân bố
Trong các nghiên cứu in vitro (trong ống nghiệm), Lorlatinib cho thấy khả năng gắn với protein huyết tương người khoảng 66%, cho thấy mức độ liên kết ở mức trung bình. Hoạt chất này chủ yếu liên kết với albumin và α1-acid glycoprotein, hai loại protein vận chuyển quan trọng trong huyết tương.
Chuyển hóa
Ở người, Lorlatinib được chuyển hóa chủ yếu thông qua hai con đường chính là oxy hóa và glucuronid hóa. Các nghiên cứu in vitro cho thấy quá trình chuyển hóa của thuốc chủ yếu liên quan đến enzyme CYP3A4 và UGT1A4, trong khi các enzyme CYP2C8, CYP2C19, CYP3A5 và UGT1A3 chỉ tham gia với mức độ nhỏ hơn.
Trong huyết tương, một chất chuyển hóa quan trọng của Lorlatinib là dẫn xuất acid benzoic, được tạo thành thông qua quá trình phân cắt oxy hóa các liên kết amid và ether thơm trong cấu trúc phân tử của thuốc. Chất chuyển hóa này chiếm khoảng 21% tổng lượng phóng xạ lưu hành trong tuần hoàn. Tuy nhiên, nghiên cứu cho thấy chất chuyển hóa này không có hoạt tính dược lý, do đó không đóng góp vào hiệu quả điều trị của thuốc.
Thải trừ
Sau khi dùng một liều Lorlatinib 100 mg, thời gian bán thải trung bình trong huyết tương của thuốc khoảng 23,6 giờ, cho thấy hoạt chất được đào thải tương đối chậm khỏi cơ thể. Trong nghiên cứu sử dụng Lorlatinib được đánh dấu phóng xạ, tổng lượng chất đánh dấu thu hồi trung bình đạt khoảng 88,6%, trong đó 47,7% được bài tiết qua nước tiểu và 40,9% qua phân.
Trong huyết tương và phân của người, Lorlatinib ở dạng không biến đổi vẫn là thành phần chính, chiếm lần lượt khoảng 44% và 9,1% tổng lượng phóng xạ được phát hiện. Ngược lại, lượng Lorlatinib nguyên vẹn trong nước tiểu rất thấp, dưới 1%, cho thấy phần lớn thuốc được đào thải sau khi đã trải qua quá trình chuyển hóa.
Ngoài ra, Lorlatinib còn có khả năng cảm ứng enzyme chuyển hóa thuốc thông qua việc hoạt hóa thụ thể pregnane X (PXR) và thụ thể androstane cấu thành (CAR) ở người.
Tương tác thuốc
Lorlatinib có thể xảy ra nhiều tương tác thuốc do ảnh hưởng đến hệ enzyme chuyển hóa, đặc biệt là CYP3A4/5, vì vậy cần thận trọng khi phối hợp với các thuốc khác.
Các chất cảm ứng mạnh CYP3A4/5 có thể làm giảm đáng kể nồng độ Lorlatinib trong huyết tương. Ngoài ra còn ghi nhận tăng men gan AST và ALT. Vì vậy, việc dùng đồng thời Lorlatinib với các chất cảm ứng mạnh CYP3A4/5 như rifampicin, carbamazepine, enzalutamide, mitotane, phenytoin hoặc Hypericum perforatum (cây ban âu) được chống chỉ định. Đối với các chất cảm ứng CYP3A4/5 mức độ vừa phải, tác động thường ít nghiêm trọng hơn.
Ngược lại, các chất ức chế mạnh CYP3A4/5 có thể làm tăng nồng độ Lorlatinib trong máu. Những thuốc như ketoconazole, posaconazole, voriconazole, ritonavir hoặc các thuốc kháng virus kết hợp có thể gây tăng nồng độ thuốc tương tự. Sản phẩm từ bưởi cũng có thể làm tăng nồng độ Lorlatinib nên cần tránh. Trong trường hợp bắt buộc phải dùng chung với chất ức chế mạnh CYP3A4/5, cần cân nhắc giảm liều Lorlatinib.
Ngoài việc bị ảnh hưởng bởi thuốc khác, Lorlatinib cũng có thể tác động đến chuyển hóa của nhiều thuốc dùng kèm. Hoạt chất này là chất cảm ứng CYP3A mức độ vừa phải, do đó có thể làm giảm nồng độ của các thuốc là chất nền CYP3A4/5. Vì vậy nên tránh phối hợp với các thuốc có chỉ số điều trị hẹp như alfentanil, ciclosporin, dihydroergotamine, ergotamine, fentanyl, pimozide, quinidine, sirolimus, tacrolimus hoặc thuốc tránh thai nội tiết, do nguy cơ giảm hiệu quả của các thuốc này.
Đối với các chất nền UGT, Lorlatinib có thể làm giảm nồng độ thuốc. Ví dụ, khi phối hợp với acetaminophen, AUC giảm khoảng 45%. Ngoài ra, Lorlatinib còn là chất cảm ứng P-glycoprotein (P-gp) mức độ vừa phải, làm giảm nồng độ của các thuốc là chất nền P-gp. Trong nghiên cứu, AUC của fexofenadine giảm khoảng 67% khi dùng cùng Lorlatinib. Vì vậy, cần thận trọng khi phối hợp với các thuốc P-gp có chỉ số điều trị hẹp như digoxin hoặc dabigatran etexilate, do nguy cơ làm giảm nồng độ thuốc trong huyết tương.
Chống chỉ định
Lorlatinib chống chỉ định ở bệnh nhân có tiền sử quá mẫn với Lorlatinib hoặc với bất kỳ thành phần nào của thuốc.
Liều lượng & cách dùng
Liều dùng
Người lớn
Liều khuyến cáo của Lorlatinib là 100 mg uống một lần mỗi ngày. Thuốc được dùng đều đặn hằng ngày và có thể uống cùng hoặc không cùng thức ăn.
Việc điều trị bằng Lorlatinib thường được duy trì liên tục cho đến khi bệnh không còn đáp ứng hoặc xuất hiện độc tính không thể chấp nhận được. Trong suốt quá trình điều trị, bệnh nhân cần được theo dõi lâm sàng và xét nghiệm định kỳ để đánh giá hiệu quả cũng như độ an toàn của thuốc.
Trong một số trường hợp, bác sĩ có thể tạm ngừng hoặc giảm liều tùy theo mức độ tác dụng phụ và khả năng dung nạp của từng bệnh nhân. Các mức giảm liều thường được áp dụng như sau:
- Giảm liều lần thứ nhất: 75 mg, uống một lần mỗi ngày.
- Giảm liều lần thứ hai: 50 mg, uống một lần mỗi ngày.
Nếu bệnh nhân không dung nạp được liều 50 mg mỗi ngày, việc điều trị bằng Lorlatinib nên ngừng vĩnh viễn.
Trẻ em
Tính an toàn và hiệu quả của Lorlatinib ở bệnh nhân dưới 18 tuổi hiện vẫn chưa được xác định. Cho đến nay chưa có đủ dữ liệu lâm sàng để đánh giá mức độ an toàn hoặc hiệu quả điều trị của thuốc trong nhóm đối tượng này. Vì vậy, việc sử dụng Lorlatinib cho trẻ em chưa được khuyến cáo.
Cách dùng
Lorlatinib được sử dụng đường uống. Người bệnh nên uống thuốc vào cùng một thời điểm mỗi ngày để duy trì nồng độ thuốc ổn định trong cơ thể. Thuốc có thể dùng cùng hoặc không cùng bữa ăn.
Viên thuốc cần được nuốt nguyên viên với nước, không được nhai, nghiền hoặc bẻ viên trước khi uống vì có thể ảnh hưởng đến quá trình giải phóng và hấp thu hoạt chất. Không nên sử dụng các viên thuốc bị vỡ, nứt hoặc không còn nguyên vẹn để đảm bảo an toàn và hiệu quả điều trị.
Tác dụng phụ
Tác dụng phụ rất phổ biến
Các phản ứng bất lợi rất phổ biến khi sử dụng Lorlatinib chủ yếu liên quan đến rối loạn chuyển hóa, thần kinh và toàn thân. Người bệnh có thể gặp tình trạng tăng cholesterol máu, tăng triglyceride máu, phù nề, bệnh thần kinh ngoại biên, tăng cân, rối loạn nhận thức, mệt mỏi, khó thở, đau khớp, tiêu chảy, thay đổi tâm trạng, ho, đau cơ, thiếu máu, đau đầu, buồn nôn, táo bón, rối loạn thị giác, chóng mặt, tăng men gan (ALT, AST), phát ban da, nôn, tăng huyết áp, tăng lipase, rối loạn giấc ngủ và tăng amylase. Phần lớn các phản ứng này có mức độ nhẹ đến trung bình nhưng cần được theo dõi trong quá trình điều trị.
Tác dụng phụ phổ biến
Các tác dụng không mong muốn thường gặp khác bao gồm tăng đường huyết, thay đổi giọng nói, tăng creatine phosphokinase trong máu, các biểu hiện loạn thần, tăng gamma-glutamyl peptidase, protein niệu, block nhĩ thất, viêm phổi và thay đổi trạng thái tinh thần. Những biểu hiện này có thể liên quan đến ảnh hưởng của thuốc lên hệ thần kinh, gan, tim mạch hoặc quá trình chuyển hóa.
Tác dụng phụ hiếm gặp
Một số phản ứng bất lợi hiếm gặp cũng đã được ghi nhận khi dùng Lorlatinib, trong đó đáng chú ý là viêm tụy. Mặc dù xảy ra với tần suất thấp, tình trạng này có thể nghiêm trọng, vì vậy cần theo dõi các dấu hiệu như đau bụng dữ dội, buồn nôn hoặc nôn kéo dài trong quá trình sử dụng thuốc.
Lưu ý
Lưu ý chung
Trong quá trình điều trị bằng Lorlatinib, người bệnh cần được theo dõi chặt chẽ để hạn chế nguy cơ xảy ra các tác dụng không mong muốn và đảm bảo hiệu quả điều trị. Một số lưu ý quan trọng bao gồm:
- Theo dõi nồng độ lipid máu định kỳ vì thuốc có thể gây tăng cholesterol và triglyceride.
- Kiểm tra chức năng thần kinh và tâm thần do thuốc có thể gây rối loạn nhận thức, thay đổi tâm trạng hoặc các biểu hiện thần kinh trung ương khác.
- Theo dõi huyết áp trong suốt quá trình điều trị vì có nguy cơ gây tăng huyết áp.
- Đánh giá chức năng gan thông qua xét nghiệm men gan định kỳ để phát hiện sớm các dấu hiệu tổn thương gan.
- Thận trọng khi sử dụng đồng thời với các thuốc có khả năng tương tác qua hệ enzyme CYP, đặc biệt là CYP3A4/5.
- Theo dõi các dấu hiệu rối loạn tim mạch, bao gồm block nhĩ thất hoặc thay đổi nhịp tim.
- Bệnh nhân cần thông báo cho bác sĩ nếu xuất hiện các triệu chứng bất thường như chóng mặt, thay đổi hành vi, khó thở, đau ngực hoặc phù nề trong quá trình dùng thuốc.
Lưu ý với phụ nữ có thai
Các nghiên cứu trên động vật cho thấy Lorlatinib có thể gây độc tính đối với phôi và thai nhi. Hiện chưa có đủ dữ liệu về độ an toàn của thuốc khi sử dụng ở phụ nữ mang thai. Do đó, việc dùng Lorlatinib trong thai kỳ có nguy cơ gây ảnh hưởng bất lợi đến sự phát triển của thai nhi. Thuốc không nên sử dụng cho phụ nữ đang mang thai, trừ khi lợi ích điều trị vượt trội so với nguy cơ tiềm ẩn. Phụ nữ trong độ tuổi sinh sản cần áp dụng biện pháp tránh thai hiệu quả trong thời gian điều trị để hạn chế nguy cơ phơi nhiễm thuốc cho thai nhi.
Lưu ý với phụ nữ cho con bú
Hiện chưa có dữ liệu xác định liệu Lorlatinib hoặc các chất chuyển hóa của thuốc có bài tiết vào sữa mẹ hay không. Tuy nhiên, không thể loại trừ khả năng thuốc có thể gây ảnh hưởng bất lợi cho trẻ bú mẹ. Vì lý do an toàn, không nên sử dụng Lorlatinib trong thời gian cho con bú. Nếu cần điều trị bằng thuốc này, người mẹ nên ngừng cho trẻ bú trong suốt quá trình điều trị và ít nhất 7 ngày sau liều cuối cùng.

Lưu ý khi lái xe và vận hành máy móc
Lorlatinib có thể ảnh hưởng ở mức độ vừa phải đến khả năng lái xe và vận hành máy móc. Trong quá trình điều trị, một số bệnh nhân có thể gặp các tác dụng không mong muốn liên quan đến hệ thần kinh trung ương, như chóng mặt, rối loạn nhận thức hoặc thay đổi tâm trạng. Những triệu chứng này có thể làm giảm sự tỉnh táo và khả năng tập trung, do đó người bệnh cần thận trọng khi lái xe, vận hành máy móc hoặc thực hiện các công việc đòi hỏi sự chú ý cao trong thời gian sử dụng thuốc.
Quá liều
Quá liều và xử trí
Quá liều và độc tính
Hiện chưa có nhiều dữ liệu lâm sàng về tình trạng quá liều Lorlatinib ở người. Khi dùng quá liều, bệnh nhân có thể gặp gia tăng mức độ và tần suất của các tác dụng không mong muốn, đặc biệt là các rối loạn liên quan đến hệ thần kinh trung ương, rối loạn chuyển hóa lipid, tăng huyết áp, rối loạn tiêu hóa hoặc tăng men gan. Do thuốc có thời gian bán thải tương đối dài, các biểu hiện bất lợi có thể kéo dài và cần được theo dõi cẩn thận.
Cách xử lý khi quá liều
Trong trường hợp nghi ngờ quá liều Lorlatinib, cần ngừng thuốc ngay lập tức và đưa người bệnh đến cơ sở y tế để được theo dõi. Hiện không có thuốc giải độc đặc hiệu cho Lorlatinib, do đó việc điều trị chủ yếu là điều trị hỗ trợ và xử trí triệu chứng. Bác sĩ có thể theo dõi các dấu hiệu sinh tồn, chức năng gan, tình trạng thần kinh và các xét nghiệm sinh hóa cần thiết để kiểm soát biến chứng.
Quên liều và xử trí
Nếu quên một liều Lorlatinib, người bệnh nên uống ngay khi nhớ ra. Tuy nhiên, nếu thời điểm nhớ ra còn dưới 4 giờ trước liều kế tiếp, nên bỏ qua liều đã quên và tiếp tục dùng thuốc theo lịch trình bình thường. Không nên dùng gấp đôi liều để bù cho liều đã bỏ lỡ nhằm tránh nguy cơ tăng tác dụng phụ.
- EMC: https://www.medicines.org.uk/emc/product/10701/smpc
- Drugbank: https://go.drugbank.com/drugs/DB12130
:format(webp)/Option_1_2_2d9677e5fd.png)
:format(webp)/Option_1_1_2a84e0cd00.png)
