Thuốc Xeomin 100 Units Merz điều trị loạn trương lực cơ cổ, co thắt mi, co cứng sau đột quỵ chi trên
Thuốc Xeomin là sản phẩm của Merz Pharma, có thành phần chính là Độc tố thần kinh Clostridium botulinum type A. Đây là thuốc được sử dụng để điều trị loạn trương lực cơ cổ, co thắt mi, co cứng sau đột quỵ chi trên, các nếp nhăn cau mày ở vùng điểm giữa trên gốc mũi ở người lớn.
Số đăng ký
Quy cách
Thành phần
Xem tất cả thông tin
Lưu ý: Sản phẩm này chỉ bán khi có chỉ định của bác sĩ, mọi thông tin trên Website chỉ mang tính chất tham khảo.
Thuốc Xeomin 100 Units là gì?
Kích thước chữ
Mặc định
Lớn hơn
Công dụng của Thuốc Xeomin 100 Units
Chỉ định
Thuốc Xeomin được chỉ định dùng trong các trường hợp sau:
- Loạn trương lực cơ cổ ở người lớn.
- Co thắt mi ở người lớn.
- Co cứng sau đột quỵ chi trên ở người lớn.
- Các nếp nhăn cau mày ở vùng điểm giữa trên gốc mũi ở người lớn.
Dược lực học
Nhóm dược lý trị liệu: Thuốc giãn cơ khác, thuốc tác dụng ngoại biên.
Mã ATC: M03AX01.
Độc tố thần kinh botulinum type A phong bế sự dẫn truyền cholinergic ở khớp thần kinh cơ bằng cách ức chế sự phóng thích acetylcholin từ đầu tận cùng dây thần kinh cholinergic ngoại biên. Sự ức chế này xảy ra theo trình tự sau đây:
- Chuỗi nặng của độc tố gắn vào đầu tận cùng dây thần kinh cholinergic.
- Thu nhận độc tố trong các túi vào đầu tận cùng dây thần kinh.
- Chuyển vị chuỗi nhẹ của phân tử độc tố vào dung dịch bào tương của đầu tận cùng dây thần kinh.
- Phân cắt SNAP25 bằng enzym, một protein đích trước synap cần thiết cho sự phóng thích acetylcholin.
Sự phục hồi hoàn toàn chức năng đĩa cuối/sự dẫn truyền xung động sau khi tiêm bắp thường xảy ra trong vòng 3-4 tháng khi đầu tận cùng dây thần kinh phát triển và kết nối lại với đĩa cuối của cơ và cơ chế phóng thích chất dẫn truyền thần kinh trước synap có chức năng trở lại.
Dược động học
Các nghiên cứu về hấp thu, phân bố, chuyển hóa và thải trừ kinh điển không thể được tiến hành với độc tố thần kinh botulinum type A vì hoạt chất được sử dụng với lượng nhỏ đến mức không thể thực hiện như vậy (picogram mỗi lần tiêm) và do nó gắn kết rất nhanh và không hồi phục với đầu tận cùng dây thần kinh cholinergic.
Các nghiên cứu về dược động học trên người với Xeomin đã không được thực hiện vì những lý do được nêu chi tiết ở trên.
Cách dùng Thuốc Xeomin 100 Units
Xeomin chỉ có thể được sử dụng bởi các bác sĩ thực hành y khoa có trình độ và kinh nghiệm đã được chứng minh thích hợp trong việc sử dụng độc tố botuli-num và sử dụng các thiết bị cần thiết.
Do sự khác nhau về đơn vị trong thử nghiệm về LD50 (Liều gây chết 50% động vật thí nghiệm), đơn vị Xeomin đặc hiệu cho Xeomin. Vì vậy liều đơn vị được khuyến cáo cho Xeomin không thể hoán đổi với liều đơn vị đối với các chế phẩm độc tố botulinum khác. Do đó, một đơn vị của Xeomin không tương đương với một đơn vị của các chế phẩm độc tố botulinum khác.
Kết quả nghiên cứu lâm sàng so sánh cho thấy Xeomin và sản phẩm so sánh chứa phức hợp độc tố botulinum A thông thường (900 kDa) có hiệu lực như nhau khi sử dụng trong một tỷ lệ chuyển đổi liều 1:1.
Pha lo thuốc
Sản phẩm chỉ sử dụng một lần cho một bệnh nhân duy nhất. Loại bỏ bất kỳ lượng thuốc thừa nào.
Xeomin được pha trước khi sử dụng với dung dịch natri chlorid 9 mg/ml (0,9%) để tiêm. Cần sử dụng một kim vô khuẩn thích hợp để tiêm.
Việc pha loãng có thể thực hiện được trình bày trong bảng dưới đây:
50 đơn vị LD50 Dung môi được thêm vào (dung dịch tiêm natri chlorid 9 mg/ml (0,9%)) | 100 đơn vị LD50 Dung môi được thêm vào (dung dịch tiêm natri chlorid 9 mg/ml (0,9%)) | Liều thu được tính bằng đơn vị mỗi 0,1 ml |
|---|---|---|
0,25 ml | 0,5 ml | 20,0 đơn vị |
0,5 ml | 1,0 ml | 10,0 đơn vị |
1,0 ml | 2,0 ml | 5,0 đơn vị |
2,0 ml | 4,0 ml | 2,5 đơn vị |
4,0 ml | 8,0 ml | 1,25 đơn vị |
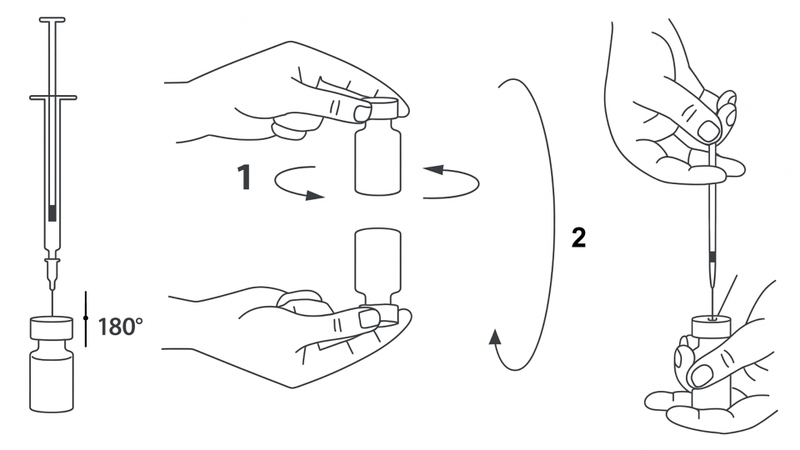
Thực hành tốt là thực hiện pha lọ thuốc và chuẩn bị ống tiêm trên khăn giấy có lớp nhựa để giữ lại bất kỳ lượng thuốc nào bị đổ ra. Rút một lượng dung môi thích hợp vào ống tiêm (xem hình dưới). Sau khi đâm kim vào theo chiều thẳng đứng xuyên qua nút cao su, bơm nhẹ nhàng dung môi vào trong lọ để tránh tạo thành bọt. Khuyến cáo nên dùng một kim ngắn 20-27 G có mặt vát để pha.
Phải loại bỏ lọ nếu chân không không kéo dung môi vào trong lọ. Rút ống tiêm ra khỏi lọ và trộn Xeomin với dung môi bằng cách cẩn thận xoáy và đảo ngược lọ - không lắc mạnh. Nếu cần thiết, nên giữ kim dùng để pha vẫn còn trong lọ và rút lượng dung dịch cần dùng bằng một ống tiêm mới phù hợp để tiêm.
Dung dịch Xeomin đã pha là một dung dịch trong suốt, không màu, không có tiểu phân. Không được sử dụng Xeomin nếu dung dịch đã pha (được chuẩn bị như trên) có vẩn đục hoặc kết cụm hoặc có tiểu phân.
Xeomin đã pha được dùng để tiêm bắp.
Loạn trương lực cơ cổ
Liều tối ưu và số lượng chỗ tiêm ở các cơ được điều trị cần được cá nhân hóa cho từng bệnh nhân và được xác định bởi bác sĩ điều trị.
Thể tích tiêm/chỗ tiêm khuyến cáo: Khoảng 0,1-0,5 ml. Thông thường, tổng liều không được vượt quá 200 đơn vị mỗi đợt điều trị. Có thể dùng liều đến tối đa 300 đơn vị. Nên dùng không quá 50 đơn vị tại một chỗ tiêm bất kỳ. Cũng như với bất kỳ điều trị bằng thuốc nào, liều khởi đầu nên bắt đầu với liều thấp nhất có hiệu quả.
Xeomin thường được tiêm vào cơ ức - đòn - chũm, cơ nâng vai, cơ gối đầu, cơ bậc thang và/hoặc cơ thang. Danh sách này không phải toàn diện vì bất kỳ cơ nào chịu trách nhiệm kiểm soát tư thế của đầu đều có thể cần phải điều trị.
Thời gian trung bình dẫn đến khởi phát hiệu lực: Trong vòng 7 ngày sau khi tiêm.
Hiệu quả của mỗi đợt điều trị thường kéo dài khoảng 3-4 tháng, tuy nhiên nó có thể kéo dài lâu hơn hoặc ngắn hơn đáng kể.
Điều trị lặp lại nói chung không nên thường xuyên hơn mỗi 6 tuần. Trong một thử nghiệm lâm sàng có đối chứng, Xeomin có hiệu quả và dung nạp tốt khi được tiêm ở các khoảng cách từ 6-20 tuần (trung bình: 12 tuần). Khoảng cách điều trị nên được xác định dựa trên nhu cầu thực tế lâm sàng của từng bệnh nhân.
Co thắt mi
Liều tối ưu và số lượng chỗ tiêm ở các cơ được điều trị cần được cá nhân hóa cho từng bệnh nhân và được xác định bởi bác sĩ điều trị.
Liều khởi đầu khuyến cáo: 1,25 - 2,5 đơn vị (thể tích 0,05 - 0,1 ml)/chỗ tiêm. Liều khởi đầu không được vượt quá 35 đơn vị/mắt đối với bệnh nhân trước khi điều trị, nếu liều trước đây của độc tố botulinum không được biết.
Liều khởi đầu không được vượt quá 25 đơn vị/mắt đối với bệnh nhân chưa từng điều trị.
Thông thường, tổng liều không được vượt quá 100 đơn vị mỗi đợt điều trị.
Điều trị lặp lại nói chung không nên thường xuyên hơn mỗi 6 tuần. Trong một thử nghiệm lâm sàng có đối chứng, Xeomin có hiệu quả và dung nạp tốt khi được tiêm ở các khoảng cách từ 6-20 tuần (trung bình: 12 tuần). Khoảng cách điều trị nên được xác định dựa trên nhu cầu thực tế lâm sàng của từng bệnh nhân.
Xeomin được tiêm vào cơ vòng mi giữa và bên của mi mắt trên và vào cơ vòng mi bên của mi mắt dưới. Các vị trí khác ở vùng lông mày, cơ vòng mi bên và vùng mặt phía trên cũng có thể được tiêm nếu sự co thắt ở đây ảnh hưởng đến thị lực.
Thời gian trung bình dẫn đến khởi phát hiệu lực đầu tiên: Trong vòng 4 ngày sau khi tiêm.
Hiệu quả của mỗi đợt điều trị thường kéo dài khoảng 3-4 tháng, tuy nhiên, nó có thể kéo dài lâu hơn hoặc ngắn hơn đáng kể ở từng bệnh nhân.
Co cứng chi trên sau đột quỵ
Liều tối ưu và số lượng chỗ tiêm ở các cơ được điều trị cần được cá nhân hóa cho từng bệnh nhân và được xác định bởi bác sĩ điều trị.
Liều khởi đầu khuyến cáo:
Mô hình lâm sàng Cơ | Đơn vị |
|---|---|
Cổ tay gập Cơ gấp xương quay cổ tay Cơ gấp xương trụ cổ tay |
50 40 |
Bàn tay nắm chặt Cơ gấp nông các ngón tay Cơ gấp sâu các ngón tay |
40 40 |
Khuỷu tay gập Cơ cánh tay - xương quay Cơ hai đầu Cơ cánh tay |
60 80 50 |
Cẳng tay quay sấp Cơ sấp vuông Cơ sấp tròn |
25 40 |
Ngón cái trong lòng bàn tay Cơ gấp dài ngón tay cái Cơ khép ngón tay cái Cơ gấp ngắn ngón tay cái/Cơ đối ngón tay cái |
20 10 10 |
Liều khuyến cáo đối với điều trị lặp lại:
Mô hình lâm sàng Cơ | Đơn vị (khoảng) | Số lượng chỗ tiêm mỗi cơ |
|---|---|---|
Cổ tay gập Cơ gấp xương quay cổ tay Cơ gấp xương trụ cổ tay |
25-100 20-100 |
1-2 1-2 |
Bàn tay nắm chặt Cơ gấp nông các ngón tay Cơ gấp sâu các ngón tay |
40-100 40-100 |
2 2 |
Khuỷu tay gập Cơ cánh tay - xương quay Cơ hai đầu Cơ cánh tay |
25-100 75-200 25-100 |
1-3 1-4 1-2 |
Cẳng tay quay sấp Cơ sấp vuông Cơ sấp tròn |
10-50 25-75 |
1 1-2 |
Ngón cái trong lòng bàn tay Cơ gấp dài ngón tay cái Cơ khép ngón tay cái Cơ gấp ngắn ngón tay cái/Cơ đối ngón tay cái |
10-50 5-30 5-30 |
1 1 1 |
Tổng liều tối đa khuyến cáo: Tối đa 400 đơn vị mỗi đợt điều trị. Thời gian trung bình dẫn đến khởi phát hiệu quả đầu tiên: Trong vòng 4 ngày sau khi tiêm. Hiệu quả tối đa dưới dạng cải thiện trương lực cơ: Trong vòng 4 tuần. Nhìn chung, hiệu quả điều trị kéo dài 12 tuần. Điều trị lặp lại nói chung không nên thường xuyên hơn mỗi 12 tuần.
Liều lượng chính xác và số lượng chỗ tiêm cần được điều chỉnh theo từng bệnh nhân dựa trên kích thước, số lượng cơ và sự khu trú của cơ liên quan, mức độ nặng của sự co cứng và sự hiện diện yếu cơ tại chỗ.
Các nếp nhăn cau mày ở vùng điểm giữa trên gốc mũi
Liều tối ưu và số lượng chỗ tiêm ở các cơ được điều trị cần được cá nhân hóa cho từng bệnh nhân và được xác định bởi bác sĩ điều trị.
Liều lượng
Pha: 50 đơn vị/1,25 ml
Thể tích tiêm khuyến cáo: 0,1 ml (4 đơn vị) vào mỗi chỗ trong 5 chỗ tiêm: 2 mũi tiêm vào mỗi cơ cau mày và một mũi tiêm trong cơ tháp của mũi.
Liều chuẩn là 20 đơn vị. Liều này có thể được tăng lên bởi bác sĩ đến tối đa 30 đơn vị nếu cần theo nhu cầu riêng của từng bệnh nhân. Sự cải thiện các nếp nhăn cau mày ở vùng điểm giữa trên gốc mũi: Thường là trong vòng 2-3 ngày.
Hiệu quả tối đa: Vào ngày thứ 30. Hiệu quả kéo dài đến 4 tháng sau khi tiêm.
Khoảng cách giữa các lần điều trị: ≥ 3 tháng.
Cách dùng
Để làm giảm nguy cơ sa mi mắt, phải tránh tiêm gần cơ nâng mi trên và vào phần sọ của cơ vòng mi. Tiêm vào cơ cau mày nên được thực hiện ở phần giữa của cơ và ở phần trung tâm của bụng cơ ít nhất 1 cm trên rìa xương của hốc mắt.
Lưu ý: Liều dùng trên chỉ mang tính chất tham khảo. Liều dùng cụ thể tùy thuộc vào thể trạng và mức độ diễn tiến của bệnh. Để có liều dùng phù hợp, bạn cần tham khảo ý kiến bác sĩ hoặc chuyên viên y tế.
Làm gì khi dùng quá liều?
Dấu hiệu và triệu chứng:
Tăng liều độc tố thần kinh Botulinum type A có thể dẫn đến liệt thần kinh cơ rõ rệt xa chỗ tiêm với một loạt các triệu chứng (triệu chứng có thể bao gồm yếu toàn thân, sa mi mắt, song thị, khó thở, khó khăn về nói, liệt cơ hô hấp hoặc khó nuốt có thể dẫn đến viêm phổi sặc). Các triệu chứng của quá liều không phải rõ ràng ngay lập tức sau khi tiêm.
Cách xử trí:
Trong trường hợp quá liều, bệnh nhân phải được theo dõi y tế về các triệu chứng yếu cơ hoặc liệt cơ quá mức. Điều trị triệu chứng có thể cần thiết. Có thể cần hỗ trợ hô hấp nếu xảy ra liệt cơ hô hấp.
Trong trường hợp khẩn cấp, hãy gọi ngay cho Trung tâm cấp cứu 115 hoặc đến trạm Y tế địa phương gần nhất.
Làm gì khi quên 1 liều?
Bổ sung liều ngay khi nhớ ra. Tuy nhiên, nếu thời gian giãn cách với liều tiếp theo quá ngắn thì bỏ qua liều đã quên và tiếp tục lịch dùng thuốc. Không dùng liều gấp đôi để bù cho liều đã bị bỏ lỡ.
Tác dụng phụ
Khi sử dụng thuốc Xeomin bạn có thể gặp các tác dụng không mong muốn (ADR):
Các phản ứng bất lợi được báo cáo theo chỉ định
Dựa trên thông tin từ kinh nghiệm lâm sàng về tần suất của các phản ứng bất lợi đối với các chỉ định riêng biệt được nêu dưới đây. Các nhóm tần suất được xác định như sau: rất thường gặp (≥ 1/10); thường gặp (≥ 1/100 đến < 1/10); hiếm gặp (≥ 1/1.000 đến < 1/100), hiếm gặp (≥ 1/10.000 đến < 1/1.000); rất hiếm gặp (< 1/10.000).
Loạn trương lực cơ cổ
Rối loạn tiêu hóa:
- Rất thường gặp: Khó nuốt.
- Ít gặp: Khô miệng, buồn nôn.
Rối loạn toàn thân:
- Thường gặp: Đau tại chỗ tiêm.
- Ít gặp: Suy nhược.
Rối loạn hệ cơ xương và mô liên kết:
- Thường gặp: Đau cổ, yếu cơ, đau cơ xương khớp, cứng cơ xương khớp.
- Ít gặp: Co thắt cơ.
Rối loạn hệ thần kinh:
- Thường gặp: Nhức đầu.
- Ít gặp: Sắp ngất, chóng mặt, rối loạn về nói.
Rối loạn hô hấp, ngực và trung thất:
- Ít gặp: Khó phát âm, khó thở.
- Không rõ: Nhiễm trùng đường hô hấp trên.
Rối loạn da và mô dưới da:
- Ít gặp: Tăng tiết mồ hôi, phát ban.
Lưu ý: Dựa trên các nghiên cứu lâm sàng đối chứng với giả dược, đối chứng với hoạt chất và không đối chứng.
Co thắt mi
Rối loạn hệ thần kinh:
- Ít gặp: Nhức đầu.
- Không rõ: Liệt nhẹ mặt.
Rối loạn mắt:
- Thường gặp: Sa mi mắt, khô mắt, nhìn mờ.
- Ít gặp: Suy giảm thị lực, song thị, tăng chảy nước mắt.
Rối loạn tiêu hóa:
- Thường gặp: Khô miệng.
- Ít gặp: Khó nuốt.
Rối loạn toàn thân:
- Thường gặp: Đau tại chỗ tiêm.
- Ít gặp: Mệt mỏi.
Rối loạn hệ cơ xương và mô liên kết:
- Ít gặp: Yếu cơ.
Lưu ý: Dựa trên các nghiên cứu lâm sàng đối chứng với giả dược, đối chứng với hoạt chất và không đối chứng.
Co cứng chi trên sau đột quỵ
Rối loạn tiêu hóa:
- Ít gặp: Khó nuốt.
Rối loạn toàn thân:
- Ít gặp: Suy nhược, cảm giác nóng.
Rối loạn hệ cơ xương và mô liên kết:
- Thường gặp: Yếu cơ.
- Ít gặp: Đau ở chi.
- Không rõ: Đau cơ.
Rối loạn hệ thần kinh:
- Ít gặp: Nhức đầu, loạn cảm, giảm cảm giác.
Lưu ý: Dựa trên các nghiên cứu lâm sàng đối chứng với giả dược, đối chứng với hoạt chất và không đối chứng.
Các nếp nhăn cau mày ở vùng điểm giữa trên hốc mũi
Rối loạn toàn thân:
- Ít gặp: Khối tụ máu tại chỗ tiêm, đau tại chỗ tiêm.
- Hiếm gặp: Bệnh giống cúm, nhạy cảm đau, mệt mỏi.
Rối loạn hệ cơ xương và mô liên kết:
- Ít gặp: Cảm giác nặng.
- Hiếm gặp: Co thắt cơ.
Rối loạn hệ thần kinh:
- Thường gặp: Nhức đầu.
- Ít gặp: Liệt nhẹ mặt (xệ lông mày).
Rối loạn mắt:
- Ít gặp: Phù mí mắt.
- Hiếm gặp: Nhìn mờ, sa mí mắt.
Rối loạn da và mô dưới da:
- Ít gặp: Ngứa.
Nhiễm trùng và nhiễm ký sinh trùng:
- Hiếm gặp: Viêm mũi họng.
Lưu ý: Dựa trên các nghiên cứu lâm sàng đối chứng với giả dược, đối chứng với hoạt chất và không đối chứng.
Tác dụng bất lợi liên quan đến việc tiêm
Như được dự kiến đối với bất kỳ thủ thuật tiêm nào, đau khu trú, viêm, dị cảm, giảm cảm giác, nhạy cảm đau, sưng, phù, ban đỏ, ngứa, nhiễm trùng khu trú, khối tụ máu, chảy máu và/hoặc bầm tím có thể liên quan với việc tiêm.
Đau và/hoặc lo âu liên quan đến kim tiêm có thể dẫn đến đáp ứng mạch - thần kinh phế vị, bao gồm hạ huyết áp triệu chứng thoáng qua, lo âu, buồn nôn, ù tai và ngất.
Tác dụng bất lợi liên quan đến nhóm dược lý
Yếu cơ khu trú là một trong những tác dụng dược lý được dự kiến của độc tố botulinum.
Lan truyền độc tố
Khi điều trị trong các chỉ định về thần kinh, các tác dụng phụ liên quan đến việc lan truyền độc tố xa chỗ tiêm đã được báo cáo rất hiếm gặp (yếu cơ quá mức, khó nuốt, viêm phổi sặc với kết quả gây tử vong).
Các tác dụng không mong muốn như trên không thể được loại trừ hoàn toàn khi sử dụng Xeomin trong các chỉ định về thẩm mỹ.
Khó nuốt
Việc xử trí loạn trương lực cơ cổ có thể gây ra khó nuốt với mức độ nặng khác nhau kèm khả năng hít sặc có thể đòi hỏi phải can thiệp y tế. Khó nuốt có thể kéo dài 2-3 tuần sau khi tiêm, nhưng đã có báo cáo một trường hợp kéo dài 5 tháng. Khó nuốt dường như phụ thuộc vào liều dùng.
Phản ứng quá mẫn
Phản ứng quá mẫn nghiêm trọng và/hoặc tức thì hiếm gặp đã được báo cáo, bao gồm phản vệ, bệnh huyết thanh, nổi mề đay, phù mô mềm và khó thở.
Một số trong các phản ứng này đã được báo cáo sau khi sử dụng phức hợp độc tố botulinum A thông thường đơn độc hoặc kết hợp với các thuốc khác đã biết là gây ra phản ứng tương tự.
Kinh nghiệm hậu mãi
Các triệu chứng giống cúm và phản ứng quá mẫn như sưng, phù (cũng cách xa chỗ tiêm), ban đỏ, ngứa, phát ban (tại chỗ và toàn thân) và khó thở đã được báo cáo.
Hướng dẫn cách xử trí ADR:
Thông báo cho thầy thuốc các tác dụng không mong muốn gặp phải khi sử dụng thuốc.
Lưu ý
Trước khi sử dụng thuốc bạn cần đọc kỹ hướng dẫn sử dụng và tham khảo thông tin bên dưới.
Chống chỉ định
Thuốc Xeomin chống chỉ định trong các trường hợp sau:
- Quá mẫn với hoạt chất hoặc với bất kỳ tá dược nào của thuốc.
- Rối loạn hoạt động cơ toàn thân (ví dụ nhược cơ, hội chứng Lambert-Eaton).
- Nhiễm trùng hoặc viêm tại chỗ định tiêm.
- Các trường hợp thận trọng khi dùng thuốc.
Thận trọng khi sử dụng
Trước khi sử dụng Xeomin, bác sĩ phải tự mình làm quen với giải phẫu của bệnh nhân và bất kỳ thay đổi nào về giải phẫu do các thủ thuật phẫu thuật trước đó.
Nếu chỗ định tiêm được đánh dấu bằng bút, thuốc này không được tiêm qua dấu của bút; nếu không thì tác dụng xăm vĩnh viễn có thể xảy ra.
Cần phải cẩn thận để đảm bảo là Xeomin không được tiêm vào mạch máu.
Xeomin cần được tiêm cẩn thận khi tiêm tại các c chỗ gần các cấu trúc nhạy cảm, như động mạch cảnh, đỉnh phổi và thực quản.
Cần thận trọng khi sử dụng Xeomin:
- Nếu xảy ra rối loạn chảy máu ở bất kỳ dạng nào.
- Ở những bệnh nhân đang được điều trị bằng thuốc chống đông hoặc đang dùng các chất khác ở liều thuốc chống đông.
Sự lan rộng về tác dụng của độc tố tại chỗ và đi xa
Không được vượt quá liều lượng và số lần dùng Xeomin được khuyến cáo. Liều cao hoặc không thích hợp ngoài khoảng liều khuyến cáo có thể dẫn đến tăng nguy cơ tác dụng bất lợi. Các tác dụng không mong muốn có thể xảy ra do việc tiêm độc tố thần kinh Botulinum type A không đúng chỗ làm liệt tạm thời các nhóm cơ lân cận.
Đã có báo cáo về các tác dụng không mong muốn có thể liên quan đến sự lan rộng của độc tố đến các vị trí xa chỗ tiêm. Các triệu chứng phù hợp với cơ chế tác dụng của độc tố botulinum và có thể bao gồm suy nhược, yếu cơ toàn thân, song thị, nhìn mờ, sa mi mắt, khó nuốt, khó phát âm, loạn vận ngôn, tiểu không tự chủ và khó thở. Những triệu chứng này đã được báo cáo trong vòng vài giờ đến vài tuần sau khi tiêm. Khó nuốt và khó thở có thể đe dọa tính mạng và đã có báo cáo về tử vong liên quan đến sự lan rộng về tác dụng của độc tố.
Nguy cơ gặp các triệu chứng có lẽ là lớn nhất ở trẻ em được điều trị co cứng nhưng các triệu chứng có thể xảy ra ở người lớn điều trị co cứng và các tình trạng khác, đặc biệt là ở những bệnh nhân có các tình trạng từ trước làm cho họ dễ gặp những triệu chứng này. Về các sử dụng không được phê duyệt, bao gồm co cứng ở trẻ em và người lớn, và các chỉ định đã được phê duyệt, các triệu chứng phù hợp với sự lan rộng về tác dụng của độc tố đã được báo cáo ở các liều tương đương hoặc thấp hơn liều được sử dụng để điều trị loạn trương lực cơ cổ.
Bệnh nhân được điều trị với liều trị liệu có thể gặp yếu cơ quá mức.
Nên khuyên bệnh nhân hoặc người chăm sóc tìm sự chăm sóc y tế ngay lập tức nếu xảy ra rối loạn về nuốt, rối loạn về nói hoặc rối loạn hô hấp.
Khó nuốt cũng đã được báo cáo sau khi tiêm vào các vị trí khác ngoài hệ thống cơ cổ.
Rối loạn thần kinh cơ có từ trước
Những bệnh nhân bị rối loạn thần kinh cơ có thể tăng nguy cơ bị yếu cơ quá mức. Sản phẩm độc tố botulinum nên được sử dụng ở những bệnh nhân này dưới sự giám sát của bác sĩ chuyên khoa và chỉ nên được sử dụng nếu lợi ích điều trị được cho là lớn hơn nguy cơ.
Những bệnh nhân đang được điều trị trong các chỉ định về thần kinh có tiền sử khó nuốt và hít sặc cần được điều trị cực kỳ thận trọng.
Việc sử dụng Xeomin trong các chỉ định về thẩm mỹ không được khuyến cáo cho những bệnh nhân có tiền sử nuốt khó và hít sặc.
Cần thận trọng khi sử dụng Xeomin:
- Ở bệnh nhân bị xơ cứng cột bên teo cơ.
- Ở bệnh nhân bị các bệnh khác dẫn đến rối loạn chức năng thần kinh cơ ngoại biên.
- Ở các cơ đích có biểu hiện yếu hoặc teo rõ rệt.
Phản ứng quá mẫn
Phản ứng quá mẫn đã được báo cáo với sản phẩm độc tố botulinum. Nếu xảy ra phản ứng quá mẫn nghiêm trọng (ví dụ phản ứng phản vệ) và/hoặc quá mẫn tức thì, phải tiến hành điều trị y tế thích hợp.
Sự hình thành kháng thể
Sự hình thành các kháng thể trung hòa đối với độc tố thần kinh Clostridium botulinum type A (150 kDa) không có các protein tạo phức hợp có thể làm giảm hiệu quả điều trị bằng Xeomin do làm bất hoạt hoạt tính sinh học của độc tố. Các yếu tố quan trọng đối với sự hình thành kháng thể trung hòa chưa được mô tả rõ. Dùng các liều quá thường xuyên có thể làm tăng nguy cơ hình thành kháng thể, có thể dẫn đến thất bại điều trị ngay cả khi sản phẩm đang được sử dụng để điều trị trong các chỉ định khác. Khả năng hình thành kháng thể có thể được giảm thiểu bằng cách tiêm với liều thấp nhất có hiệu quả ở những khoảng cách thấp nhất có thể thực hiện được giữa các mũi tiêm.
Không có khả năng hoán đổi cho nhau giữa các sản phẩm độc tố botulinum
Các đơn vị hoạt lực của Xeomin đặc hiệu cho chế phẩm và phương pháp thử nghiệm sử dụng. Chúng không thể hoán đổi với các chế phẩm khác của sản phẩm độc tố botulinum và do đó các đơn vị hoạt tính sinh học của Xeomin không thể được so sánh hoặc chuyển đổi thành đơn vị của bất kỳ sản phẩm độc tố botulinum nào khác được đánh giá bằng bất kỳ phương pháp thử nghiệm đặc hiệu nào khác.
Loạn trương lực cơ cổ
Cần thông báo cho bệnh nhân là việc tiêm Xeomin để điều trị loạn trương lực cơ cổ có thể gây ra khó nuốt từ nhẹ đến nặng với nguy cơ hít sặc và khó thở.
Những bệnh nhân bị khó nuốt hoặc khó thở từ trước có thể nhạy cảm hơn với những biến chứng này. Trong hầu hết các trường hợp, đây là hậu quả của sự yếu cơ trong vùng tiêm có liên quan đến thở hoặc nuốt. Khi xảy ra tác dụng ở xa, các cơ hô hấp phụ có thể liên quan.
Các trường hợp tử vong như là một biến chứng của khó nuốt nặng đã được báo cáo sau khi điều trị bằng độc tố botulinum. Khó nuốt có thể kéo dài trong vài tháng và đòi hỏi phải sử dụng một ống thông nuôi ăn để duy trì dinh dưỡng và bù nước đầy đủ. Hít sặc có thể do khó nuốt nặng và là một nguy cơ đặc biệt khi điều trị cho những bệnh nhân có chức năng nuốt hoặc chức năng hô hấp đã bị tổn thương.
Điều trị loạn trương lực cơ cổ bằng độc tố botulinum có thể làm yếu các cơ cổ đóng vai trò như cơ hô hấp phụ. Điều này có thể dẫn đến việc mất khả năng thở nguy cấp ở những bệnh nhân bị rối loạn hô hấp mà có thể đã trở nên phụ thuộc vào các cơ hô hấp phụ này. Đã có báo cáo hậu mãi về khó thở nghiêm trọng, bao gồm cả suy hô hấp ở những bệnh nhân bị loạn trương lực cơ cổ được điều trị bằng sản phẩm độc tố botulinum.
Những bệnh nhân có khối cơ cổ nhỏ hơn và những bệnh nhân cần các mũi tiêm hai bên vào cơ ức - đòn - chũm đã được báo cáo là có nguy cơ lớn hơn về khó nuốt. Nói chung, hạn chế liều tiêm vào cơ ức - đòn - chũm có thể làm giảm sự xuất hiện khó nuốt.
Những bệnh nhân được điều trị bằng độc tố botulinum có thể cần phải có sự chăm sóc y tế ngay lập tức nếu họ phát sinh các vấn đề với rối loạn về nuốt, rối loạn về nói hoặc rối loạn hô hấp. Những phản ứng này có thể xảy ra trong vòng vài giờ đến vài tuần sau khi tiêm độc tố botulinum.
Co thắt mi
Nên tránh tiêm gần cơ nâng mi trên để giảm sự xuất hiện sa mi mắt. Song thị có thể phát sinh do sự khuếch tán của độc tố thần kinh Botulinum type A vào cơ chéo dưới. Việc tránh tiêm vào vùng mí mắt dưới phía trong có thể làm giảm phản ứng bất lợi này.
Việc giảm chớp mắt sau khi tiêm sản phẩm độc tố botulinum vào cơ vòng mi có thể dẫn đến bộc lộ giác mạc, khuyết tật biểu mô kéo dài và loét giác mạc, đặc biệt ở bệnh nhân bị rối loạn dây thần kinh số VII. Cần kiểm tra cẩn thận cảm giác giác mạc ở mắt đã được phẫu thuật trước đó, tránh tiêm vào vùng mí mắt dưới để tránh lộn mi và điều trị tích cực mọi khuyết tật của biểu mô. Điều này có thể đòi hỏi phải dùng thuốc nhỏ mắt, thuốc mỡ tra mắt, kính sát tròng mềm dùng trong điều trị để bảo vệ, hoặc khép mắt bằng băng dính, hoặc bằng các phương tiện khác. Do tác dụng kháng cholinergic, cần thận trọng khi sử dụng Xeomin cho những bệnh nhân có nguy cơ phát sinh glaucoma góc hẹp. Để phòng ngừa lộn mi, không nên tiêm sản phẩm độc tố botulinum vào vùng mí mắt dưới phía trong.
Bầm máu dễ xảy ra ở các mô mềm của mí mắt. Ấn nhẹ ngay tại chỗ tiêm có thể hạn chế nguy cơ này.
Nguy cơ sa mi mắt ở bệnh nhân được điều trị bằng Xeomin đối với các nếp nhăn vùng điểm giữa trên gốc mũi
Không được vượt quá liều lượng và số lần dùng Xeomin được khuyến cáo.
Để làm giảm biến chứng sa mi mắt, cần thực hiện các bước sau đây:
- Tránh tiêm gần cơ nâng mi trên, đặc biệt ở những bệnh nhân có phức hợp cơ hạ lông mày lớn hơn.
- Việc tiêm ở cơ cau mày cần phải đặt ở vị trí ít nhất là 1 cm trên xương cung mày.
Albumin người và sự lây truyền bệnh do virus
Thuốc này chứa một lượng nhỏ albumin người. Nguy cơ lây nhiễm virus hoặc bệnh lây nhiễm liên quan đến prion như bệnh Creutzfeldt-Jakob (CJD) không thể loại trừ với sự chắc chắn tuyệt đối sau khi sử dụng máu người hoặc các sản phẩm của máu người.
Ảnh hưởng đến khả năng sinh sản
Chưa có dữ liệu lâm sàng về việc sử dụng độc tố thần kinh botulinum type A.
Khả năng sinh sản ở thỏ đực và cái không bị ảnh hưởng sau khi tiêm bắp liều Xeomin bắt đầu 2 tuần trước khi giao phối và tiêm mỗi 2 tuần ở mức liều ≤ 3,5 LDU/kg với tổng số 5 liều ở thỏ đực và 3 liều ở thỏ cái. Tỷ lệ phơi nhiễm tương đối là gấp 1,3 lần liều tối đa khuyến cáo cho người đối với thỏ cái và gấp 2,2 lần liều tối đa khuyến cáo cho người đối với thỏ đực về co cứng chi trên sau đột quỵ (400 đơn vị) trên cơ sở liều dùng theo thể trọng.
Sử dụng ở trẻ em
Xeomin chưa được nghiên cứu ở trẻ em và do đó không được khuyến cáo sử dụng ở nhóm tuổi trẻ em.
Sử dụng ở người cao tuổi
Không có biện pháp phòng ngừa thêm về việc sử dụng Xeomin ở nhóm bệnh nhân cao tuổi.
Sử dụng ở bệnh nhân suy thận, suy gan hoặc suy tim mạch
Không có thông tin về việc sử dụng Xeomin ở nhóm bệnh nhân này.
Độc tính gen
Chưa có nghiên cứu về độc tính gen được thực hiện với Xeomin.
Khả năng gây ung thư
Chưa có nghiên cứu dài hạn về khả năng gây ung thư ở động vật được thực hiện với thuốc tiêm Xeomin.
Ảnh hưởng của thuốc lên khả năng lái xe và vận hành máy móc
Chưa có nghiên cứu được thực hiện về tác động trên khả năng lái xe và vận hành máy móc.
Bệnh nhân cần được tư vấn rằng nếu mất sức lực, yếu cơ, nhìn mờ, mệt mỏi, chóng mặt hoặc sụp mí mắt xảy ra, họ nên tránh lái xe hoặc tham gia vào các hoạt động khác có khả năng gây nguy hiểm.
Sử dụng thuốc cho phụ nữ trong thời kỳ mang thai và cho con bú
Chưa có dữ liệu đầy đủ về việc sử dụng độc tố thần kinh botulinum type A ở phụ nữ có thai. Các nghiên cứu trên động vật đã cho thấy độc tính đối với sinh sản. Chưa rõ nguy cơ tiềm ẩn đối với người. Không nên sử dụng Xeomin trong khi mang thai trừ khi thật sự cần thiết.
Không có bằng chứng về tính sinh quái thai trong các nghiên cứu ở động vật. Tuy nhiên, Xeomin cho thấy tác dụng bất lợi nhỏ đến sự phát triển của phôi - thai ở chuột cống và tăng sẩy thai ở thỏ khi được dùng với liều cao hơn khoảng 10 lần liều tối đa khuyến cáo cho người (MRHD) đối với chuột cống và cao hơn khoảng 2 lần liều tối đa khuyến cáo cho người (MRHD) đối với thỏ về co cứng chi trên sau đột quỵ (400 đơn vị) trên cơ sở liều dùng theo thể trọng. Ý nghĩa của phát hiện này được xem là không chắc chắn ở người và phù hợp với những phát hiện đã được báo cáo đối với các thuốc độc tố thần kinh botulinum type A khác.
Khi tiêm bắp Xeomin cho chuột cống mang thai trong giai đoạn hình thành cơ quan (tức là tổng cộng 3 mũi tiêm ở liều 3, 10 hoặc 30 đơn vị/kg vào những ngày mang thai [GD] 6, 12, 19; hoặc 14 mũi tiêm ở liều 7 đơn vị/kg vào những ngày mang thai 6-19; hoặc 5 mũi tiêm ở liều 2, 6 hoặc 18 đơn vị/kg vào những ngày mang thai 6, 9, 12, 16, 19), đã quan sát thấy giảm trọng lượng thai và sự cốt hóa xương ở liều không độc cho chuột mẹ. Mức liều không quan sát thấy tác dụng có hại đối với sự phát triển của phôi-thai ở chuột cống là một tổng liều 90-98 LDU/kg [tức là 14 mũi tiêm ở liều 7 LDU/kg hoặc 3 mũi tiêm ở liều 30 LDU/kg hoặc 5 mũi tiêm ở liều 18 LDU/kg (gấp 11,25-12,25 lần liều tối đa khuyến cáo cho người (MRHD) đối với co cứng chi trên sau đột quỵ trên cơ sở liều dùng theo thể trọng).
Tiêm bắp Xeomin cho thỏ mang thai trong giai đoạn hình thành cơ quan (1,25, 2,5 hoặc 5 đơn vị/kg vào những ngày mang thai 6, 18 và 28) đã dẫn đến tăng tỷ lệ sẩy thai ở mức liều gây độc cho thỏ mẹ là 5 đơn vị/kg. Ở thỏ, mức liều không quan sát thấy tác dụng có hại về sẩy thai là 2,5 đơn vị/kg [phơi nhiễm tương đối gấp 0,9 lần lần liều tối đa khuyến cáo cho người (MRHD) đối với co cứng chi trên sau đột quỵ (400 đơn vị) trên cơ sở liều dùng theo thể trọng.
Sử dụng ở phụ nữ cho con bú
Chưa rõ liệu độc tố thần kinh botulinum tube A có được bài tiết vào sữa mẹ hay không. Việc sử dụng Xeomin trong khi cho con bú không được khuyến cáo.
Tương tác thuốc
Việc dùng đồng thời Xeomin và kháng sinh nhóm aminoglycoside hoặc các thuốc khác can thiệp vào sự dẫn truyền thần kinh cơ, ví dụ thuốc giãn cơ nhóm tubocurarin, chỉ nên được thực hiện với sự thận trọng vì những thuốc này có thể làm tăng tác dụng của độc tố.
Bảo quản
Lo chưa mở
Bảo quản dưới 30°C.
Dung dịch đã pha
Để làm giảm nguy cơ về vi sinh vật, sử dụng càng sớm càng tốt sau khi pha.
Nếu việc bảo quản là cần thiết, giữ dung dịch đã pha ở 2-8°C không quá 24 giờ.
Quy trình cần tuân theo để loại bỏ an toàn các lọ, ống tiêm và vật liệu đã sử dụng
Bất kỳ lọ thuốc nào không sử dụng, dung dịch đã pha còn lại trong lọ và/hoặc ống tiêm nên được bất hoạt bằng cách thêm vào một trong những dung dịch sau: Ethanol 70%, isopropanol 50%, dung dịch natri hydroxid loãng (NaOH 0,1 N), hoặc dung dịch natri hypochlorit loãng (ít nhất là NaOCl 0,1%).
Các lọ, ống tiêm và vật liệu đã sử dụng không nên làm rỗng và cần được loại bỏ vào thùng chứa thích hợp và hủy bỏ phù hợp với yêu cầu của địa phương.
Mọi thông tin trên đây chỉ mang tính chất tham khảo. Việc sử dụng thuốc phải tuân theo hướng dẫn của bác sĩ chuyên môn.
Dược sĩ chuyên khoa Dược lý - Dược lâm sàng. Tốt nghiệp 2 trường đại học Mở và Y Dược TP. Hồ Chí Minh. Có kinh nghiệm nghiên cứu về lĩnh vực sức khỏe, đạt được nhiều giải thưởng khoa học. Hiện là Dược sĩ chuyên môn phụ trách xây dựng nội dung và triển khai dự án đào tạo - Hội đồng chuyên môn tại Nhà thuốc Long Châu.
Câu hỏi thường gặp
Cần làm gì nếu gặp các triệu chứng của quá liều Xeomin?
Tăng liều có thể dẫn đến liệt thần kinh cơ rõ rệt xa chỗ tiêm với các triệu chứng như yếu toàn thân, sa mi mắt, song thị, khó thở, hoặc liệt cơ hô hấp. Nếu quá liều xảy ra, bệnh nhân phải được theo dõi y tế về các triệu chứng yếu cơ quá mức. Có thể cần hỗ trợ hô hấp nếu xảy ra liệt cơ hô hấp.
Thuốc Xeomin được dùng theo đường nào và ai có thể thực hiện tiêm thuốc?
Xeomin đã pha được dùng để tiêm bắp. Thuốc chỉ có thể được sử dụng bởi các bác sĩ thực hành y khoa có trình độ và kinh nghiệm đã được chứng minh thích hợp trong việc sử dụng độc tố botulinum và các thiết bị cần thiết.
Cách pha loãng và chuẩn bị thuốc Xeomin như thế nào?
Xeomin được pha trước khi sử dụng với dung dịch natri chlorid 9 mg/ml (0,9%) để tiêm. Khi pha, cần bơm nhẹ nhàng dung môi vào lọ để tránh tạo thành bọt. Phải trộn bằng cách cẩn thận xoáy và đảo ngược lọ - không lắc mạnh. Dung dịch đã pha phải trong suốt, không màu, không có tiểu phân.
Cơ chế tác dụng của Xeomin là gì?
Xeomin (Độc tố thần kinh botulinum type A) hoạt động bằng cách phong bế sự dẫn truyền cholinergic ở khớp thần kinh cơ. Nó ức chế sự phóng thích acetylcholin từ đầu tận cùng dây thần kinh cholinergic ngoại biên bằng cách phân cắt SNAP25, một protein cần thiết cho sự phóng thích chất dẫn truyền thần kinh.
Thuốc Xeomin được chỉ định dùng trong những trường hợp bệnh lý nào?
Thuốc Xeomin được chỉ định dùng trong các trường hợp sau:
- Loạn trương lực cơ cổ ở người lớn.
- Co thắt mi ở người lớn.
- Co cứng sau đột quỵ chi trên ở người lớn.
- Các nếp nhăn cau mày ở vùng điểm giữa trên gốc mũi ở người lớn.
Đánh giá sản phẩm

Hãy sử dụng sản phẩm và trở thành người đầu tiên đánh giá trải nghiệm nha.
Hỏi đáp (0 bình luận)
Lọc theo:
Mai Quỳnh Trâm AnhDược sĩ
Chào Chị Nguyệt,
Hiện tại, sản phẩm XEOMIN 100 UNITS MERZ có hỗ trợ xuất VAT ạ.
Chị có thể gửi yêu cầu Tư vấn ngay trên website hoặc tại ứng dụng Long Châu/ZALO OA Nhà thuốc FPT Long Châu để hưởng ưu đãi miễn phí vận chuyển khi đặt giao tại nhà ạ.
1 tháng trướcHữu ích
Trả lời
- TT
Trần thị thuận
Xeomin còn ko , có giá bao nhiêu ạk1 tháng trướcHữu ích
Trả lờiTrịnh Thu NgaDược sĩ
Chào chị Thuận,
Hiện tại sản phẩm XEOMIN 100 UNITS MERZ có giá 5,600,000 ₫/hộp ạ
Chị có thể gửi yêu cầu Tư vấn ngay trên website hoặc tại ứng dụng Long Châu / ZALO OA Nhà thuốc FPT Long Châu để hưởng ưu đãi miễn phí vận chuyển khi đặt giao tại nhà, tích điểm và đổi quà ạ
1 tháng trướcHữu ích
Trả lời
- CN
c Nụ
thuốc này còn không ạ3 tháng trướcHữu ích
Trả lờiTrần Lê Hải BìnhDược sĩ
Chào chị Nụ,
Tư vấn viên nhà thuốc Long Châu sẽ sớm liên hệ với chị qua số điện thoại đã cung cấp để hỗ trợ thêm ạ.
3 tháng trướcHữu ích
Trả lời
- HT
Phạm Thị Hồng Thủy
xin giá sản phẩm6 tháng trướcHữu ích
Trả lờiNguyễn Thị Ngọc ChâuDược sĩ
Chào bạn Phạm Thị Hồng Thủy,
Hiện tại, sản phẩm có giá 5,250,000 ₫/lọ.
Tư vấn viên nhà thuốc Long Châu sẽ sớm liên hệ với bạn qua số điện thoại đã cung cấp để hỗ trợ thêm ạ.
6 tháng trướcHữu ích
Trả lời
:format(webp)/DSC_05280_56567b5788.png)
:format(webp)/Left_item_112x150_897a6dd499.png)
:format(webp)/Right_item_112x150_9ef5853f7e.png)
:format(webp)/BG_e5cebbb9d2.png)
:format(webp)/Bg_Header_LV_2_74ff94c12b.png)
:format(webp)/smalls/Left_item_68x52_ee5ad23e00.png)

:format(webp)/smalls/Right_item_68x52_1bd962bdfb.png)
:format(webp)/smalls/Badge_52ad415e46.png)
:format(webp)/DSC_05280_56567b5788.png)
:format(webp)/DSC_05282_454b7312c8.png)
:format(webp)/DSC_05283_2176389e5d.png)
:format(webp)/DSC_05284_e4dda416f7.png)
:format(webp)/DSC_05274_c762f0fd37.png)
:format(webp)/DSC_05277_8a79edd3fe.png)
:format(webp)/DSC_05279_a2be6fe3d1.png)
:format(webp)/DSC_05273_a85b1fa044.png)
:format(webp)/DSC_05275_09438123d2.png)
:format(webp)/DSC_05276_be817439f7.png)
:format(webp)/xeomin1_81b6701b23.jpg)
:format(webp)/xeomin2_681bdcc106.jpg)
:format(webp)/xeomin3_69fd899673.jpg)
:format(webp)/xeomin4_6b3a1c930f.jpg)
:format(webp)/xeomin5_3887088f0d.jpg)
:format(webp)/xeomin6_eb676687c7.jpg)
:format(webp)/xeomin7_74b3bc4c69.jpg)
:format(webp)/xeomin8_42c2218d9f.jpg)
:format(webp)/xeomin9_64ad742a8e.jpg)
:format(webp)/xeomin10_0c0a58f4fa.jpg)
:format(webp)/xeomin11_6aace58476.jpg)
:format(webp)/xeomin12_967e61dadb.jpg)
:format(webp)/xeomin13_fdde18f372.jpg)
:format(webp)/xeomin14_36e9644106.jpg)
:format(webp)/xeomin15_5db2f1473c.jpg)
:format(webp)/xeomin16_68094317a8.jpg)
:format(webp)/xeomin17_4abcc7442a.jpg)
:format(webp)/xeomin18_0f46534968.jpg)
:format(webp)/DSC_05280_56567b5788.png)
:format(webp)/DSC_05282_454b7312c8.png)
:format(webp)/DSC_05283_2176389e5d.png)
:format(webp)/DSC_05284_e4dda416f7.png)
:format(webp)/DSC_05274_c762f0fd37.png)
:format(webp)/DSC_05279_a2be6fe3d1.png)
:format(webp)/DSC_05273_a85b1fa044.png)
:format(webp)/DSC_05275_09438123d2.png)
:format(webp)/DSC_05276_be817439f7.png)
:format(webp)/xeomin1_81b6701b23.jpg)
:format(webp)/xeomin2_681bdcc106.jpg)
:format(webp)/xeomin3_69fd899673.jpg)
:format(webp)/xeomin4_6b3a1c930f.jpg)
:format(webp)/xeomin5_3887088f0d.jpg)
:format(webp)/xeomin6_eb676687c7.jpg)
:format(webp)/xeomin7_74b3bc4c69.jpg)
:format(webp)/xeomin8_42c2218d9f.jpg)
:format(webp)/xeomin9_64ad742a8e.jpg)
:format(webp)/xeomin10_0c0a58f4fa.jpg)
:format(webp)/xeomin11_6aace58476.jpg)
:format(webp)/xeomin12_967e61dadb.jpg)
:format(webp)/xeomin13_fdde18f372.jpg)
:format(webp)/xeomin14_36e9644106.jpg)
:format(webp)/xeomin15_5db2f1473c.jpg)
:format(webp)/xeomin16_68094317a8.jpg)
:format(webp)/xeomin17_4abcc7442a.jpg)
:format(webp)/xeomin18_0f46534968.jpg)
Trịnh Thị Nguyệt
Hữu ích
Trả lời