Thuốc Cellcept 250mg Roche dự phòng hiện tượng thải ghép cấp tính (10 vỉ x 10 viên)
Thuốc Cellcept 250mg được bào chế dưới dạng viên nang chứa hoạt chất Mycophenolate Mofetil (MMF), được sản xuất bởi Roche S.p.A. Cellcept 250mg được dùng điều trị ở những bệnh nhân ghép thận, NMF giúp cải thiện khả năng sống trong năm đầu tiền sau khi được ghép tim.
Số đăng ký
Quy cách
Thành phần
Xem tất cả thông tin
Lưu ý: Sản phẩm này chỉ bán khi có chỉ định của bác sĩ, mọi thông tin trên Website chỉ mang tính chất tham khảo.
Thuốc Cellcept 250mg là gì?
Kích thước chữ
Mặc định
Lớn hơn
Công dụng của Thuốc Cellcept 250mg
Chỉ định
- Cellcept được chỉ định để dự phòng hiện tượng thải ghép cấp tính và để điều trị tình trạng thải ghép lần đầu hoặc đáp ứng kém với điều trị ở những bệnh nhân ghép thận không cùng hệ thống.
- Cellcept được chỉ định để dự phòng hiện tượng thải ghép cấp tính ở những bệnh nhân ghép tim không cùng huyết thống. Ở những bệnh nhân được điều trị, NMF giúp cải thiện khả năng sống trong năm đầu tiền sau khi được ghép tim.
- Cellcept được chỉ định để dự phòng thải ghép cấp tính ở những bệnh nhân ghép gan không cùng huyết thống.
- Cellcept cần được sử dụng đồng thời với Cyclosporin và Corticosteroid.
Dược lực học
Cơ chế tác dụng
Mycophenolate mofetil (MMF) là dạng este 2-morpholinoethyl của mycophenolic axit (MPA).
MPA là một chất ức chế enzym inosine monophosphate dehydrogenase (IMPDH) với tính chất ức chế mạnh, chọn lọc, không cạnh tranh và có khả năng phục hồi, vì vậy, thuốc ức chế con đường de novo của quá trình tổng hợp guanosine nucleotide.
Cơ chế MPA ức chế hoạt tính enzyme của IMPDH dường như làdo MPA có khả năng bắt chước về mặt cấu trúc của cả đồng yếu tố nicotinamide adenine dinucleotide lẫn một phân tử nước xúc tác. Điều này sẽ ngăn cản sự oxy hoá IMP thành xanthose-5 -monophosphate là bước chính trong con đường denovo của quá trình tổng hợp guanosine nucleotide.
MPA có tác dụng kìm hãm dòng lympho bào mạnh hơn đối với các dòng tế bào khác bởi vì tế bào lympho T và lympho B bị lệ thuộc rất nhiều vào sự tăng sinh của chúng trong con đường de novo của quá trình tổng hợp purines, trong khi những dòng tế bào khác có thể tận dụng những con đường tái tạo khác.
Những nghiên cứu về hiệu quả lâm sàng
Trong các thử nghiệm lâm sàng về điều trị dự phòng các giai đoạn thải trừ mảnh ghép trong ghép thận, tim và gan, CellCept đã được dùng phối hợp với globulin kháng tế bào tuyến ức, OKT3, ciclosporin và corticosteroids để điều trị những giai đoạn thải ghép thận khó điều trị.
Trước khi điều trị với CellCept, bệnh nhân đã được dùng globulin kháng tế bào lympho, globulin kháng tế bào tuyến ức và OKT3. Sau đó, CellCept được sử dụng cùng với daclizumab và tacrolimus trong những thử nghiệm lâm sàng này.
Dự phòng thai ghép tạng
Bệnh nhân trưởng thành:
Tính an toàn và hiệu quả của CellCept khi dùng phối hợp với corticosteroid và ciclosporin để điều trị dự phòng thải ghép tạng đã được đánh giá ở những bệnh nhân được ghép thận trong ba thử nghiệm ngẫu nhiên, mù đối, đa trung tâm; ở những bệnh nhân được ghép tim trong một thử nghiệm ngẫu nhiên, mù đội, đa trung tâm; và ở những bệnh nhân được ghép gan trong một thử nghiệm ngẫu nhiên, mù đôi, đa trung tâm.
Bệnh nhi:
An toàn, dược động học, hiệu quả điều trị của CellCept trong phối hợp điều trị với corticosteroid và ciclosporin trong phòng chống thải ghép ở bệnh nhi ghép thận được đánh giá trong nghiên cứu nhãn mở, đa trung tâm trên 100 bệnh nhân (tuổi từ 3 tháng – 18 tuổi)
Ghép thận
Bệnh nhân trưởng thành:
Ba thử nghiệm so sánh hai mức liều dùng đường uống của CellCept (1g x 2 lần mỗi ngày và 1,5g x 2 lần mỗi ngày) kết hợp với azathioprine (2 thử nghiệm) hoặc giả dược (1 thử nghiệm) và dùng phối hợp với ciclosporin và corticosteroid để điều trị dự phòng những giai đoạn thải ghép cấp tính.
Kết cuộc chính về hiệu quả của thuốc là tỷ lệ số bệnh nhân trong từng nhóm trị liệu bị thất bại với điều trị trong vòng 6 tháng đầu sau khi ghép tạng (thất bại với điều trị được xác định khi: Có sự thải ghép cấp trong quá trình điều trị được khẳng định qua sinh thiết; hoặc khi bệnh nhân tử vong hoặc mất tạng ghép; hoặc khi bệnh nhân phải kết thúc sớm, không theo tiếp được cuộc thử nghiệm vì bất kỳ lý do nào, mà không có tình trạng thải ghép được khẳng định qua sinh thiết trước đó).
CellCept được nghiên cứu trong ba liệu trình điều trị sau: (1) cho dùng globulin kháng tế bào tuyến ức/sau đó dùng MMF hoặc azathioprine/ciclosporin/corticosteroids, (2) MMF hoặc azathioprine/ciclosporin/corticosteroids, và (3) MMF hoặc giả dược/ciclosporin/corticosteroids.
CellCept, khi phối hợp với corticosteroids và ciclosporin làm giảm (có ý nghĩa về mặt thống kê ở mức <0,05) tỷ lệ thất bại với điều trị trong vòng 6 tháng đầu sau khi ghép tạng.
Bảng dưới đây tóm tắt kết quả của những thử nghiệm này.
Những bệnh nhân phải ngừng điều trị sớm đã được theo dõi về tình trạng tử vong hoặc mất tạng ghép, và người ta đã tóm tắt riêng rẽ tỷ lệ lũy tích tình trạng mất tạng ghép và tình trạng tử vong.
Những bệnh nhân phải ngừng điều trị sớm đã không được theo dõi về tình trạng thải ghép cấp tính sau khi ngưng thuốc.
Số bệnh nhân trong nhóm dùng CellCept phải ngưng điều trị (không có tình trạng thải ghép được khẳng định qua sinh thiết trước đó, tử vong hoặc mất tạng ghép) nhiều hơn so với số bệnh nhân phải ngưng điều trị trong nhóm chứng, với tỷ lệ cao nhất trong nhóm dùng CellCept 3g/ngày. Do đó, tỷ lệ thải ghép cấp tính có thể được đánh giá không đúng mức, đặc biệt là ở nhóm dùng CellCept 3g/ngày.
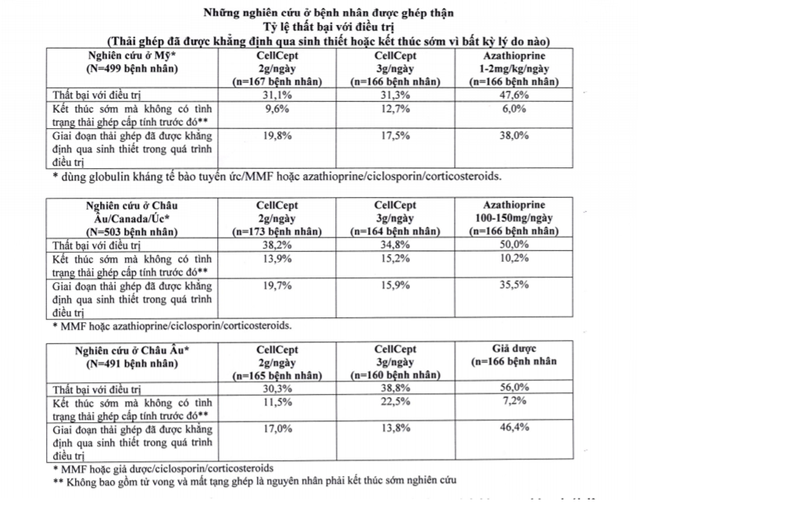
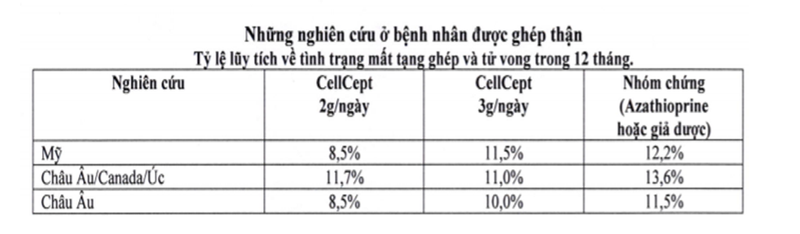
Tỷ lệ lũy tích của tình trạng mất tạng ghép và tử vong trong 12 tháng đã được trình bày trong bảng dưới đây. Không thiết lập được sự vượt trội của CellCept về tỷ lệ mất tạng ghép và tỷ lệ bệnh nhân tử vong.
Về số lượng, những bệnh nhân dùng CellCept 2g/ngày và 3g/ngày có kết quả tốt hơn so với nhóm chứng trong cả ba thử nghiệm; bệnh nhân dùng CellCept 2g/ngày có kết quả tốt hơn bệnh nhân dùng CellCept 3g/ngày trong hai trong số ba thử nghiệm này.
Những bệnh nhân phải kết thúc điều trị sớm ở tất cả các nhóm đều có kết quả kém với hiện tượng mất tạng ghép và tử vong trong vòng một năm.
Kết cục chính về hiệu quả được đo lường bằng tỷ lệ bệnh nhân xảy ra thải ghép cấp tính trong 6 tháng đầu sau cấy ghép.
Tỷ lệ thải ghép có bằng chứng mô học tương tự như trên các nhóm khác (3 tháng đến <6 tuổi, 6 tuổi đến < 12 tuổi, 12 tuổi đến < 18 tuổi). Tỷ lệ thải ghép có bằng chứng mô học toàn phần trên bệnh nhân 6 tháng tương đương với ở bệnh nhân trưởng thành.
Tỷ lệ hỏng tạng ghép (5%) và tử vong (2%) ở bệnh nhân 12 tháng tuổi sau khi ghép thận tương tự như tỷ lệ quan sát thấy trên bệnh nhân trưởng thành ghép thận.
Ghép tim
Một thử nghiệm mù đôi, ngẫu nhiên, so sánh, nhóm tương đương, đa trung tâm đã được tiến hành trên những bệnh nhân được ghép tim lần đầu. Tổng số bệnh nhân tham gia vào thử nghiệm là 650 người, trong đó có 72 người chưa bao giờ được điều trị bằng thuốc thử nghiệm và 578 người được điều trị bằng thuốc thử nghiệm.
Những bệnh nhân được dùng CellCept 1,5g x 2 lần mỗi ngày (n=289) hoặc azathioprine 1,5-3mg/kg/ngày (n=289) phối hợp với ciclosporin và corticosteroids là liệu pháp duy trì ức chế miễn dịch. Hai kết cuộc chính về hiệu quả là:
(1) tỷ lệ số bệnh nhân sau khi ghép tim có ít nhất một lần bị thải ghép đã được khẳng định qua sinh thiết cơ màng trong cơ tim có tổn hại huyết động lực, hoặc được tái ghép hoặc tử vong, trong vòng 6 tháng đầu; và (2) tỷ lệ bệnh nhân tử vong hoặc tái phép trong vòng 12 tháng sau khi được ghép tim.
Những bệnh nhân phải kết thúc điều trị sớm được theo dõi về tình trạng thải ghép dị mô trong vòng 6 tháng và về tử vong trong vòng 1 năm.
1. Thải ghép: Không có sự khác biệt nào giữa CellCept và Azathioprine (AZA) trên tình trạng thái ghép được khẳng định qua sinh thiết, có tổn hại huyết động lực, như đã được trình bày trong bảng sau:
| Thải ghép trong vòng 6 tháng | ||||
| Tất cả bệnh nhân | Bệnh nhân được điều trị | |||
AZA N=323 | Cellcept N=327 | AZA N=289 | CellCept N=289 | |
| Thải ghép được khẳng định qua sinh thiết, có tổn hại đến huyết động lực* | 121 (38%) | 120 (37%) | 100 (35%) | 92 (32%) |
Tổn hại đến huyết động lực xảy ra nếu có một trong các tiêu chuẩn sau: áp lực góc chêm mao mạch phổi 220mm hoặc tăng 25%; chỉ số tim 2,0l/phútm hoặc giảm 25%, phân suất tống máu <30%; độ bão hòa oxy động mạch phổi<60% hoặc giảm 25%; mới xuất hiện tiếng ngựa phi Sở; thu ngắn phân đoạn<20% hoặc giảm 25%; cần phải được hỗ trợ co cơ tim để cải thiện tình trạng lâm sàng.
2. Sống sót: Ở những bệnh nhân tham gia vào thử nghiệm, không có sự khác biệt có ý nghĩa thống kê về tình trạng tử vong và tái ghép tim giữa nhóm bệnh nhân được chọn ngẫu nhiên để điều trị với MMF và nhóm bệnh nhân được chọn ngẫu nhiên để điều trị với AZA.
Ở những bệnh nhân được dùng thuốc thử nghiệm, giới hạn dưới của 97,5% khoảng tin cậy của sự khác biệt giữa tử vong và tái ghép tim là 0,9 trong vòng 1 năm, cho thấy rằng MMF có ưu điểm hơn AZA ở những bệnh nhân này, điều này được trình bày ở bảng dưới đây:
| Tử vong hoặc tái ghép tim trong vòng 1 năm | ||||
| Tất cả bệnh nhân | Bệnh nhân được điều trị | |||
AZA N=323 | Cellcept N=327 | AZA N=289 | CellCept N=289 | |
| Tử vong hoặc tái ghép tim | 49 (15,2%) | 42 (12,8%) | 33 (11,4%) | 18 (6,2%) |
| Sự khác biệt về điều trị được hiệu chỉnh theo trọng số | 2,6% | 5,3% | ||
| Giới hạn dưới của 97,5% khoảng tin cậy một phía | -2,5% | +0,9% | ||
Ghép gan: Một nghiên cứu mù đôi, ngẫu nhiên, so sánh, nhóm tương đương, đa trung tâm về những bệnh nhân được ghép gan lần đầu tiên đã được tiến hành tại 16 trung tâm ở Mỹ, 2 trung tâm ở Canada, 4 trung tâm ở Châu Âu và 1 trung tâm ở Úc.
Tổng số bệnh nhân tham gia vào nghiên cứu này là 565 người và 564 người được dùng thuốc nghiên cứu. Những bệnh nhân này hoặc là được tiêm tĩnh mạch CellCept 1g x 2 lần mỗi ngày trong 14
ngày, sau đó uống CellCept 1,5g x 2 lần mỗi ngày hoặc là được tiêm tĩnh mạch azathioprine 1-2mg/kg/ngày, sau đó uống azathioprine 1-2mg/kg/ngày; kết hợp với ciclosporin và corticosteroid là liệu pháp duy trì ức chế miễn dịch.
Hai mục tiêu đánh giá chính là: (1) tỷ lệ bệnh nhân trong vòng 6 tháng đầu sau khi ghép gan có một hoặc nhiều giai đoạn thải ghép đã được khẳng định qua sinh thiết và đã được điều trị, hoặc được tái ghép hoặc tử vong; và (2) tỷ lệ bệnh nhân bị mất tạng ghép (tử vong hoặc được tái ghép) trong vòng 12 tháng sau khi được ghép gan.
Những bệnh nhân phải kết thúc điều trị sớm được theo dõi về tình trạng mất tạng ghép (tử vong hoặc được tái ghép) trong vòng 1 năm. Kết quả: Trong phân tích cơ bản (trên nhóm được dự định điều trị), CellCept dùng phối hợp với corticosteroids và ciclosporin có ưu điểm vượt trội hơn azathioprine trong việc điều trị dự, phòng thải ghép cấp tính (p=0,025) và tương đương với azathioprine trong việc duy trì sự sống cho bệnh nhân.
| Thải ghép trong vòng 6 tháng / Tử vong hoặc tái ghép trong vòng 1 năm | ||
| AZA N=287 | CellCelpt N=278 | |
| Thải ghép được khẳng định qua sinh thiết và đã được điều trị trong vòng 6 tháng | 137(47,7%) | 107(38,5%) |
| Tử vong hoặc tái phép trong vòng 1 năm | 42(14,6%) | 41(14,7%) |
Điều trị thải ghép tạng khó điều trị
Một nghiên cứu ngẫu nhiên, nhãn mở so sánh giữa MMF 3g mỗi ngày và corticosteroid tiêm tĩnh mạch đã được tiến hành trên 150 bệnh nhân được ghép thận bị thải ghép dị mô tế bào, cấp tính, khó điều trị.
Mục tiêu chính trong nghiên cứu này là tỷ lệ bệnh nhân còn sống với tạng ghép còn chức năng hoạt động trong vòng 6 tháng sau khi tham gia nghiên cứu.
Kết quả: Tỷ lệ mất tạng ghép trong nhóm chứng thấp hơn mong đợi; và phân tích cơ bản dựa trên test tỷ lệ xác suất liên tục cho thấy có xu hướng sống sót với tạng ghép được cải thiện trong nhóm dùng MMF (p=0,081).
Một phân tích phụ, sử dụng test Cochran-Mantel-Haenzel (không được điều chỉnh để theo dõi liên tục) cho thấy có sự giảm 45% tỷ lệ bị mất tạng ghép hoặc tử vong trong vòng 6 tháng sau khi tham gia nghiên cứu trong nhóm MMF (p=0,062).
| Mất tạng ghép hoặc tử vong trong vòng 6 tháng | ||
Steroids tiêm tĩnh mạch N=73 | Cellcept N=77 | |
| Mất tạng ghép hoặc tử vong trong vòng 6 tháng | 19 (26,0%) | 11 (14,3%) |
Dược động học
Dược động học của mycophenolate mofetil (MMF) đã được nghiên cứu ở những bệnh nhân ghép thận, tim và gan.
Nhìn chung, dược động học của MPA ở bệnh nhân ghép tim và ghép thận thì giống nhau. Trong giai đoạn ngay trước khi ghép, những bệnh nhân ghép gan uống một liều MMF 1,5g hoặc tiêm tĩnh mạch một liều MMF1g có nồng độ MPA tương đương so với những bệnh nhân ghép thận dùng 1g MMF đường uống hoặc đường tĩnh mạch.
Hấp thu
Sau khi được dùng theo đường uống và đường truyền, mycophenolate mofetil được hấp thu nhanh và rộng và chuyển hoàn toàn thành chất chuyển hóa có hoạt tính, đó là MPA. Sinh khả dụng trung bình của mycophenolate mofetil dùng đường uống, dựa vào AUC của MPA, là 94% so với mycophenolate mofetil dùng theo đường tĩnh mạch.
Mycophenolate mofetil có thể được đánh giá một cách hệ thống sau khi truyền tĩnh mạch. Tuy nhiên, sau khi uống, nồng độ thuốc thấp hơn mức giới hạn xác định(0,4 ng/ml).
Thời gian đầu sau khi ghép (< 40 ngày), những bệnh nhân ghép thận, tim và gan có giá trị AUC trung bình của MPA thấp hơn khoảng 30% và mức Cmax thấp hơn khoảng 40% so với khoảng thời gian sau ghép lâu hơn (sau 3-6 tháng).
Giá trị AUC của MPA đạt được sau khi dùng CellCept đường truyền tĩnh mạch 1g x hai lần mỗi ngày, với tốc độ truyền được khuyến cáo cho bệnh nhân thận ngay sau khi ghép, tương đương với AUC của MPA sau khi được dùng đường uống.
Ở những bệnh nhân ghép gan, dùng 1g Cellcept đường tĩnh mạch, hai lần mỗi ngày, sau đó uống 1,5g CellCept hai lần mỗi ngày cho thấy giá trị AUC của MPA tương đương với giá trị được ghi nhận ở những bệnh nhân ghép thận được dùng 1g CellCept hai lần mỗi ngày.
Thức ăn không ảnh hưởng đến mức độ hấp thu (AUC của MPA) của mycophenolate mofetil khi được dùng với liều 1,5g dùng ngày 2 lần cho các bệnh nhân ghép thận. Tuy nhiên, nồng độ đỉnh của MPA giảm khoảng 40% khi có mặt thức ăn.
Tương đương của dạng bào chế đường uống Tương đương sinh học của CellCept dùng đường uống đã được đánh giá. Hai viên nén 500 mg được chứng minh tương đương với 4 viên nang 250 mg.
Phân phối
Nhờ có sự tái hấp thu qua vòng tuần hoàn gan-ruột, nồng độ MPA huyết tương thường tăng lên khoảng 6-12 giờ sau khi dùng thuốc. AUC của MPA giảm đi gần 40% khi sử dụng đồng thời cholestyramine (4g ba lần một ngày) phù hợp với sự gián đoạn của vòng tái tuần hoàn gan-ruột. Ở nồng độ có tác dụng trên lâm sàng, 97% MPA gắn với albumin huyết tương.
Chuyển hóa
MPA được chuyển hóa bởi glucuronyl transferase (isoform đồng phân UGT1A9) thành dạng không hoạt tính phenolic glucuronide của MPA (MPAG). Trên in vivo, MPAG được chuyển ngược thành MPA tự do thông qua vòng tái tuần hoàn gan-ruột. Một lượng nhỏ acylglucuronide (AMPAG) cũng được hình thành.
AMPAG là chất có hoạt tính dược lý và được cho là chất gây ra một số tác dụng không mong muốn của MMF (tiêu chảy, giảm bạch cầu).
Thải trừ
Dùng mycophenolate mofetil đường uống có gắn phóng xạ có thể thu được hoàn toàn lượng thuốc đã dùng, với 93% lượng thuốc được tìm thấy trong nước tiêu và 6% được tìm thấy trong phân.
Phần lớn (khoảng 87%) của liều thuốc được thải trừ qua nước tiêu dưới dạng MPAG. Một số lượng không đáng kể (< 1% của liều) được thải trừ qua nước tiểu dưới dạng MPA
Ở các nồng độ điều trị lâm sàng, MPA và MPAG không bị đào thải bởi quá trình lọc máu. Tuy nhiên, với nồng độ MPAG cao (> 100kg/ml), một lượng nhỏ MPAG cũng bị loại bỏ. Do thuốc qua vòng tuần hoàn gan ruột, những thuốc lấy đi acid mật, ví dụ như cholestyramine, làm giảm AỤC của MPA.
Thải trừ MPA phụ thuộc vào nhiều chất vận chuyển. Vận chuyển anion hữu cơ polypeptide (OATPs) và protein 2 liên quan đến đa đề kháng thuốc (MRP2) cũng liên quan đến việc thải trừ MPA; đồng phân CATP, MRP2 và protein kháng ung thư vú (BCRP) là những chất vận chuyển liên quan đến việc bài tiết mật của glucuronides.
Protein 1 đã đề kháng thuốc (MDR1) cũng có thể vận chuyển MPA, nhưng vai trò của chất này dường như được giới hạn trong quá trình hấp thu. Ở thận MPA và các chất chuyển hóa có thể tương tác với chất vận chuyển anion hữu cơ ở thận,
Dược động học ở những đối tượng đặc biệt
Bệnh nhân bị suy thận nặng
Trong một nghiên cứu dùng liều đơn (mỗi nhóm 6 đối tượng), nồng độ AỤC trung bình của MPA được quan sát sau khi dùng đường uống ở những bệnh nhân bị suy thận mạn tính năng (mức lọc cầu thận < 25ml/phút 1,73m), ở mức cao hơn 28-75% so với nồng độ này quan sát được ở những đối tượng khỏe mạnh hay ở những bệnh nhân có suy thận mức độ nhẹ hơn.
Tuy nhiên, nồng độ trung bình AUC của MPAG khi dùng liều đơn ở những bệnh nhân suy thận nặng cao hơn gấp 3-6 lần so với những trường hợp khỏe mạnh hoặc bị suy thận nhẹ, phù hợp với sự thải trừ của MPAG qua thận đã được biết.
Dược động học khi dùng nhiều liều mycophenolate mofetil ở bệnh nhân suy thận mạn tính năng chưa được nghiên cứu.
Những bệnh nhân có chức năng thận phục hồi chậm sau ghép
Ở những bệnh nhân có chức năng thận phục hồi chậm sau ghép, AUC0-12 trung bình trong huyết tương của MPA tương đương với nồng độ ở những bệnh nhân có chức năng tạng ghép phục hồi bình thường.
Có thể có tăng nhẹ nồng độ MPA huyết tương và MPA tự do ở những bệnh nhân có chức năng thận phục hồi chậm sau ghép. Không cần điều chỉnh liều của CellCept. AUCo-12 trung bình của MPAG trong huyết tương cao gấp 2-3 lần so với những bệnh nhân có chức năng thận ghép hồi phục bình thường sau ghép thận.
Ở những bệnh nhân sau ghép thận mà tạng ghép không hồi phục chức năng, nồng độ trong huyết tương của MPAG được tích lũy; sự tích lũy của MPA, nếu có thì nhỏ hơn nhiều.
Bệnh nhân bị suy gan
Nhìn chung, dược động học của MPA và MPAG không bị ảnh hưởng bởi bệnh nhu mô gan ở những người tình nguyện bị xơ gan do rượu khi dùng MMF đường uống hoặc đường tiêm tĩnh mạch. Ảnh hưởng của bệnh gan đối với quá trình này có thể tùy theo từng bệnh cụ thể. Bệnh gan với tổn thương chủ yếu ở đường mật, ví dụ như như xơ gan ứ mật tiên phát, có thể gây ra một ảnh hưởng khác.
Bệnh nhi (< 18 tuổi)
Các thông số dược động học được đánh giá trên 55 bệnh nhi ghép thận (trong khoảng từ 1 tuổi đến 18 tuổi) sử dụng 600 mg/mo mycophenolate mofetil đường uống hai lần mỗi ngày (liều tối đa lên đến 1g hai lần mỗi ngày). Liều này đạt được giá trị AUC của MPA tương tự như trên bệnh nhân trưởng thành ghép thận dùng CellCept liệu 1g hai lần mỗi ngày trong giai đoạn sớm và muộn sau ghép thận.
Giá trị AUC của MPA giữa các nhóm tuổi tương tự nhau trong giai đoạn sớm và muộn sau ghép thận.
Người già (> 65 tuổi)
Dược động học ở người già chưa được đánh giá một cách chính thức.
Cách dùng Thuốc Cellcept 250mg
Cách dùng
CellCept cần được dùng đồng thời với Cyclosporin và Corticosteroid.
Liều dùng
Liều chuẩn để dự phòng thải ghép thận
Bệnh nhân trưởng thành:
- Liều khuyên dùng là 1g dùng đường uống hoặc truyền tĩnh mạch (thời gian truyền tối thiểu là hai giờ), hai lần mỗi ngày (dùng 2g mỗi ngày) cho những bệnh nhân ghép thận.
- Mặc dầu trong các thử nghiệm lâm sàng, mức liều 1.5g hai lần mỗi ngày (3g mỗi ngày) đã cho thấy tính an toàn và hiệu quả, nhưng sự vượt trội về hiệu quả chưa được xác định cho những bệnh nhân ghép thận.
- Nhìn chung, những bệnh nhân dùng Cellcept liều 2g/ ngày cho thấy độ an toàn cao hơn những bệnh nhân dùng Cellcept 3g/ngày.
Trẻ em (từ 3 tháng – 18 tuổi):
- Liều khuyến cáo bột pha hỗn hợp dịch uống Cellcept là 600mg/m2 hai lần mỗi ngày (liều tối đa là 2g mỗi ngày).
- Bệnh nhân với diện tích cơ thể 1.25 – 1.5m2 có thể dùng Cellcept dạng viên nang ở liều 750mg hai lần mỗi ngày (1.5g mỗi ngày).
- Bệnh nhân có diện tích cơ thể > 1.5m2 có thể dùng Cellcept dạng viên nén 1g hai lần mỗi ngày (2g mỗi ngày).
Liều chuẩn để dự phòng ghép thải tim
Bệnh nhân trưởng thành: Liều khuyên dùng cho những bệnh nhân ghép tim là 1.5g dùng đường uống hoặc truyền tĩnh mạch (thời gian truyền tối thiểu hai giờ), hai lần mỗi ngày (3g một ngày).
Bệnh nhi: Không có thông tin sử dụng thuốc trên bệnh nhi ghép tim.
Liều chuẩn để dự phòng ghép gan
Bệnh nhân trưởng thành: Liều khuyên dùng cho ngững bệnh nhân ghép gan là 1g dùng đường truyền tĩnh mạch (thời gian truyền tối thiểu hai giờ), hai lần mỗi ngày (2g một ngày); hoặc 1.5g dùng đường uống, hai lần mỗi ngày (3g một ngày)
Bệnh nhi: Không có thông tin sử dụng thuốc trên bệnh nhi ghép gan.
Liều chuẩn để điều trị hiện tượng thải ghép thận lần đầu hoặc khó điều trị
Bệnh nhân trưởng thành: Liều khuyên dùng là 1.5g dùng đường uống hoặc truyền tĩnh mạch (thời gian truyền tối thiểu hai giờ), hai lần mỗi ngày (3g một ngày).
Bệnh nhi: Không có dữ liệu điều trị hiện tượng thải ghép thận lần đầu hoặc khó điều trị trên bệnh nhi ghép thận.
Liều khởi đầu của Cellcept phải được dùng càng sớm càng tốt ngay sau khi thép thận, ghép tim hoặc ghép gan.
Các hướng dẫn dử dụng liều đặc biệt
Bệnh nhân bị giảm bạch cầu trung tính
Nếu có giảm bạch cầu trung tính (lượng bạch cầu trung tính tuyệt đối < 1.3 x 103 μl), phải ngừng dùng Cellcept hoặc phải giảm liều.
Sử dụng ở người già
Liều khuyên dùng đường uống 1g x hai lần mỗi ngày ở bệnh nhân được ghép thận và 1,5g x 2 lần mỗi ngày ở bệnh nhân được ghép tim hoặc gan là phù hợp cho những bệnh nhân già.
Bệnh nhân suy thận
Bệnh nhân suy thận nặng nên tránh dùng liều cao hơn 1g x 2 lần mỗi ngày cho những bệnh nhân được ghép thận mà bị suy thận mạn nặng (tốc độ lọc cầu thận <25ml/phút/1,73m2). Điều này không áp dụng cho khoảng thời gian ngay sau khi ghép thận hoặc sau khi điều trị sự thải ghép cấp tính hoặc thải ghép khó đáp ứng điều trị.
Không có dữ liệu về những bệnh nhân được ghép gan hoặc tim bị suy thận mạn nặng. Bệnh nhân sau ghép thận có chức năng thận hồi phục chậm Không cần phải điều chỉnh liều dùng cho những bệnh nhân sau ghép thận có chức năng thận hồi phục chậm.
Bệnh nhân suy gan
Không cần phải điều chỉnh liều dùng cho những bệnh nhân được ghép thận bị bệnh nhu mô gan nặng (xem mục Những đặc tính dược động học) Không có dữ liệu về những bệnh nhân được ghép tim bị bệnh nhu mô gan nặng.
Làm gì khi dùng quá liều?
Những báo cáo về tình trạng quá liều mycophenolate mofetil đã được ghi nhận từ những thử nghiệm lâm sàng và trong suốt thời gian thuốc được lưu hành trên thị trường.
Trong rất nhiều trường hợp quá liều được báo cáo, không thấy có những biến cố bất lợi nào được ghi nhận. Những biến cố bất lợi được báo cáo trong những trường hợp quá liều đều đã được biết đến từ trước trong các dữ liệu về tính an toàn của thuốc.
Người ta cho rằng tình trạng quá liều của mycophenolate mofetil có thể làm ức chế quá mức hệ thống miễn dịch, làm tăng tính nhạy cảm với nhiễm trùng và làm ức chế tủy xương. Nếu giảm bạch cầu đa nhân trung tính xảy ra thì cần ngưng hoặc giảm liều CellCept.
MPA không bị đào thải bởi lọc máu. Tuy nhiên, ở liều cao (nồng độ C trong huyết tương cao hơn 100kg/ml), một lượng nhỏ MPAG bị đào thải. Các thuốc làm tăng thải acid mật như cholestyramine, có thể loại bỏ MPA bằng cách tăng đào thải thuốc.
Làm gì khi quên 1 liều?
Bổ sung liều ngay khi nhớ ra. Tuy nhiên, nếu thời gian giãn cách với liều tiếp theo quá ngắn thì bỏ qua liều đã quên và tiếp tục lịch dùng thuốc. Không dùng liều gấp đôi để bù cho liều đã bị bỏ lỡ.
Tác dụng phụ
Thông báo cho bác sỹ những tác dụng không mong muốn gặp phải khi sử dụng thuốc.
Các biến cố bất lợi xảy ra khi sử dụng các thuốc ức chế miễn dịch thường rất khó xác định do sự hiện diện của bệnh đang có và sự dùng cùng một lúc nhiều thuốc khác nhau.
Lưu ý
Chống chỉ định
Không dùng thuốc Cellcept 250mg trong trường hợp sau:
- Các phản ứng dị ứng với Cellcept đã được ghi nhận. Vì vậy, Cellcept được chống chỉ định ở những bệnh nhân bị quá mẫn với mycophenolate mofeti hoặc axit mycophenolic.
- Chống chỉ định dùng Cellcept cho phụ nữ có thai do có khả năng gây đột biến và quái thai.
- Chống chỉ định dùng Cellcept cho phụ nữ có khả năng mang thai mà không sử dụng các biện pháp tránh thai hiệu quả
- Chống chỉ định dùng Cellcept cho phụ nữ cho con bú.
Thận trọng khi sử dụng
Khối u:
- Cũng như đối với tất cả những bệnh nhân sử dụng phác đồ kết hợp các thuốc ức chế miễn dịch, những bệnh nhân có sử dụng Cellcept trong phác đồ ức chế miễn dịch đều có nguy cơ bị u lympho hoặc các bệnh ác tính khác, đặc biệt là ở da.
- Nguy cơ ngày dường như có liên quan tới cường độ và thời gian điều trị ức chế miễn dịch hơn là do việc sử dụng một loại thuốc nào đó.
- Như tất cả các bệnh nhân có nguy cơ cao bị ung thư da, nên hạn chế tiếp xúc với ánh sáng mặt trời và tia cực tím bằng cách mặc quần áo bảo vệ và đeo kính chống nắng có yếu tố bảo vệ cao.
Nhiễm khuẩn:
- Sự ức chế hệ thống miễn dịch quá mức cũng có thể làm tăng tính dễ bị nhiễm trùng bao gồm nhiễm trùng cơ hội, các nhiễm khuẩn nặng đe dọa tính mạng và nhiễm trùng huyết.
- Các nhiễm trùng bao gồm cả sự tái kích hoạt virus tiềm tàng, chẳng hạn tái phát viêm gan B hoặc viêm gan C hoặc các nhiễm trùng gây ra bởi các polyomavirus.
- Một số trường hợp viêm gan do tái phát viêm gan B hoặc viêm gan C đã được ghi nhận ở những bệnh nhân có mầm bệnh được điều trị bởi các thuốc ức chế miễn dịch. Trường hợp bệnh lý chất trắng não đa ổ tiến triển (Progressive Multifocal Leukoencephalopathy – PML) liên quan tới JC virus, vài trường hợp tử vong đã được ghi nhận trên bệnh nhân điều trị bằng CellCept.
- Các ca được ghi nhận thường có nguy cơ cao cho PML, bao gồm cả điều trị ức chế miễn dịch và chức năng miễn dịch bị suy giảm.
Đối với các bệnh nhân dùng thuốc ức chế miễn dịch, các bác sỹ cần chú ý tới trường hợp PML khi chẩn đoán phân biệt ở những bệnh nhân có triệu chứng về thần kinh và cần tham khảo ý kiến của các bác sỹ chuyên khoa thần kinh.
Bệnh thận liên quan tới virus BK đã được ghi nhận trong quá trình dùng CellCept ở bệnh nhân sau ghép thận. Sự nhiễm trùng này có thể dẫn tới những hậu quả nghiêm trọng, đôi khi dẫn tới hỏng thận ghép. Theo dõi bệnh nhân giúp phát hiện những bệnh nhân có nguy cơ bệnh thận liên quan tới virus BK. Cần xem xét giảm bớt sự ức chế miễn dịch ở bệnh nhân có bằng chứng bệnh thận liên quan tới virus BK.
Hệ máu và miễn dịch:
- Một số trường hợp bất sản nguyên bào hồng cầu đơn thuần (PRCA) đã được ghi nhận trên bệnh nhân điều trị bằng CellCept có kết hợp với các thuốc ức chế miễn dịch khác.
- Cơ chế gây ra PRCA của mycophenolate mofetil hiện chưa rõ; mối liên hệ của các thuốc ức chế miễn dịch khác và sự kết hợp của chúng trong một phác đồ ức chế miễn dịch hiện cũng chưa rõ.
- Trong một số trường hợp, PRCA đã được ghi nhận là phục hồi được nếu giảm liều hoặc ngừng điều trị bằng CellCept. Tuy nhiên, ở bệnh nhân ghép tạng, nếu giảm liệu pháp ức chế miễn dịch sẽ xuất hiện nguy cơ tại mỗ ghép.
- Bệnh nhân sử dụng CellCept cần được hướng dẫn để báo cáo ngay lập tức các dấu hiệu nhiễm trùng, các vết thâm tím, chảy máu hay ức chế tủy xương.
Những bệnh nhân sử dụng CellCept cần được kiểm tra công thức máu toàn phần, mỗi tuần một lần trong tháng đầu tiên, mỗi tháng 2 lần trong tháng thứ 2 và 3, sau đó kiểm tra hàng tháng cho tới hết năm đầu tiên.
Đặc biệt, những bệnh nhân dùng CellCept cần được theo dõi để phát hiện sự giảm bạch cầu đa nhân trung tính. Tình trạng giảm bạch cầu đa nhân trung tính có thể liên quan đến việc sử dụng CellCept, các thuốc phối hợp, nhiễm vi rút hoặc do kết hợp của các nguyên nhân này.
Nếu có tình trạng giảm bạch cầu đa nhân trung tính (số lượng bạch cầu đa nhân trung tính tuyệt đối <1,3 x 103/μl), nên ngừng sử dụng CellCept hoặc giảm liều và bệnh nhân cần được theo dõi một cách cẩn thận.
Nên cho bệnh nhân biết rằng trong quá trình điều trị bằng CellCept, hiệu quả của sự tiêm chủng có thể bị giảm và nên tránh sử dụng các loại vaccine sống đã làm giảm độc lực. Có thể tiêm chủng influenza. Các bác sĩ nên tham khảo các hướng dẫn quốc gia về tiêm chủng influenza.
Dạ dày-ruột:
Do CellCept làm tăng tỉ lệ các biến cố bất lợi xảy ra ở hệ tiêu hóa, bao gồm các trường hợp ít gặp như loét đường tiêu hóa, xuất huyết và thủng, nên thận trọng khi dùng CellCept cho các bệnh nhân có bệnh của hệ tiêu hóa.
CellCept là một thuốc ức chế inosine monophosphate dehydrogenase (IMPDH), vì vậy không nên sử dụng cho bệnh nhân bị thiếu enzym hypoxanthin-guaninephosphoribosyl-transferase (HGPRT) có tính chất di truyền và hiếm gặp như hội chứng Lesch-Nyhan và Kelley- Seegmiller.
Tương tác:
Cần thận trọng khi thay đổi phác đồ điều trị từ liệu pháp có chứa các thuốc ức chế miễn dịch có thể gây ức chế tuần hoàn gan ruột của MPA như ciclosporin sang các thuốc khác không có tác dụng này như sirolimus, belatacept, hay ngược lại, do sự thay đổi phác đồ điều trị có thể làm thay đổi nồng độ MPA.
Cần thận trọng với những thuốc có thể gây ức chế chu trình gan ruột của MPA như cholestyramin, kháng sinh do khả năng làm giảm nồng độ trong huyết tương và hiệu quả của CellCept.
Người ta khuyến cáo không nên sử dụng CellCept cùng với azathioprine bởi vì cả hai thuốc này có thể làm ức chế tủy xương và sự kết hợp này chưa được nghiên cứu.
Các trường hợp đặc biệt:
Nguy cơ xảy ra các biến cố bất lợi có thể tăng trên bệnh nhân lớn tuổi như nhiễm khuẩn (bao gồm bệnh virus cự bào xâm lấn mô) và xuất huyết tiêu hóa và phù phổi khi so sánh với các bệnh nhân trẻ tuổi hơn . Chống chỉ định dùng CellCept cho phụ nữ mang thai và bà mẹ đang cho con bú.
Nên tránh dùng liều vượt quá 1g, hai lần mỗi ngày ở những bệnh nhân suy chức năng thận mạn tính năng.
Không cần điều chỉnh liều ở những bệnh nhân sau ghép tạng có chức năng thận hồi phục chậm, nhưng phải theo dõi bệnh nhân một cách cẩn thận. Không có các dữ liệu ở những bệnh nhân ghép tim hoặc ghép gan có suy thận nặng.
CellCept hỗn dịch đường uống có chứa aspartame, nguồn gốc của phenylamine (tương đương 2,78 mg/ 5 mL hỗn dịch uống). Vì vậy, cần thận trọng khi sử dụng CellCept hỗn dịch uống cho bệnh nhân mắc chứng phenylketonuria.
Tương tác thuốc
Acyclovir:
Nồng độ huyết tương của acyclovir và MPAG khi dùng cùng mycophenolate mofetil với acyclovir cao hơn khi dùng riêng rẽ từng thuốc một. Bởi vì nồng độ MPAG trong huyết tương cũng như nồng độ acyclovir hay dạng tiến chất của nó, valacyclovir, tăng khi có suy thận, có khả năng hại thuốc có sự cạnh tranh thải trừ ở ống thận và có thể gây tăng hơn nữa nồng độ cả hai thuốc.
Các thuốc kháng acid và các thuốc ức chế bơm proton (PPIs): Khi uống kém chất kháng acid như hydroxit magne và hydroxit nhôm, và PPIs, như lansoprazole và pantoprazole độ hấp thu của mycophenolate mofetil bị giảm. Khi so sánh tỷ lệ thải ghép hoặc tỷ lệ mất tạng ghép giữa bệnh nhân CellCept uống PPls với bệnh nhân không uống PPIs, không quan sát thấy sự khác biệt đáng kể.
Những dữ liệu này giúp ngoại suy kết luận này cho tất cả các thuốc kháng axit do sự giảm hấp thu khi dùng đồng thời CellCept với hydroxit magne và hydroxit nhôm được coi như thấp hơn khi dùng CellCept đồng thời với PPIs.
Cholestyramine:
Ở những người khỏe mạnh bình thường đã được dùng 4g cholestyramine ba lần một ngày trong 4 ngày sau đó dùng liều đơn 1,5 g mycophenolate mofetil, diện tích dưới đường cong của MPA giảm 40%. Nên thận trọng khi dùng cùng với các thuốc làm hạn chế vòng tái tuần hoàn gan-ruột.
Ciclosporin A:
Dược động học của ciclosporin A (CsA) không bị ảnh hưởng bởi mycophenolate mofetil. Tuy nhiên, CsA ức chế tuần hoàn gan ruột của MPA, làm giảm nồng độ MPA từ 30 – 50% ở bệnh nhân ghép thận điều trị bằng CellCept và CSA khi so sánh với bệnh nhân dùng sirolimus hay belatacept và CellCept với liều tương tự CellCept.
Ngược lại, những thay đổi về nồng độ của MPA cần được dự kiến khi chuyển sử dụng cho bệnh nhân từ CSA sang thuốc ức chế miễn dịch khác không gây ảnh hưởng lên chu trình gan ruột của MPA.
Telmisartan:
Sử dụng đồng thời telmisartan và CellCept làm giảm khoảng 30% nồng độ acid mycophenolic (MPA). Telmisartan làm thay đổi sự bài tiết của MPA do kích hoạt PPAR gamma (peroxisome proliferator kích hoạt thụ thể gamma) gây tăng hoạt động của UGT1A9.
Khi so sánh tỉ lệ thải ghép, tỉ lệ hỏng tạng ghép hay các biến cố bất lợi giữa bệnh nhân sử dụng CellCept đồng thời và không đồng thời với telmisartan, không có kết luận lâm sàng nào về dược động học DDI được quan sát thấy.
Ganciclovir:
Trên cơ sở kết quả nghiên cứu liều đơn của liều khuyên dùng mycophenolate mofetil đường uống và ganciclovir tiêm tĩnh mạch; và ảnh hưởng đã biết của suy thận đối với dược động học của mycophenolate mofetil và ganciclovir, khi dùng đồng thời các thuốc này có sự cạnh tranh về cơ chế bài tiết công thận) sẽ làm tăng nồng độ MPAG và ganciclovir.
Không có sự thay đổi đáng kể về dược động học của MPA và không cần điều chỉnh liều mycophenolate mofetil. Ở những bệnh nhân suy thận dùng đồng thời mycophenolate mofetil và ganciclovir hoặc các tiền chất của nó, ví dụ valganciclovir, cần theo dõi bệnh nhân một cách cẩn thận.
Thuốc tránh thai đường uống:
Một nghiên cứu về việc dùng cùng CellCept (1g hai lần mỗi ngày) với các thuốc tránh thai đường uống có chứa ethinylestradiol (0,02-0,04mg) và levonorgestrel (0,05-0,20mg), desogestrel (0,15mg) hoặc gestodene (0,05 – 0,10mg) được tiến hành ở 18 phụ nữ bị bệnh vẩy nến trong 3 chu kỳ kinh đã cho thấy CellCept không làm ảnh hưởng về mặt lâm sàng đến nồng độ của progesterone, LH và FSH, vì thế CellCept không có ảnh hưởng đến tác dụng ức chế rụng trứng của các thuốc tránh thai đường uống.
Dược động học của thuốc tránh thai đường uống không bị ảnh hưởng ở mức độ lâm sàng khi sử dụng đồng thời với CellCept.
Rifampicin:
Sau khi đã chỉnh đúng liều, người ta vẫn quan sát thấy có sự giảm 70% nồng độ MPA (AUC – p) khi dùng phối hợp với rifampicin ở một bệnh nhân ghép tim-phổi. Vì vậy, người ta khuyên nên theo dõi sát nồng độ MPA và cần phải điều chỉnh nồng độ CellCept cho phù hợp để duy trì hiệu quả lâm sàng khi sử dụng đồng thời hai thuốc này với nhau.
Tacrolitis:
Dùng tacrolimus đồng thời với CellCept không làm ảnh hưởng đến diện tích dưới đường cong AUC cũng như nồng độ đỉnh Cmax của MPA ở những bệnh nhân được ghép gan. Trong một nghiên cứu gần đây, người ta thấy điều này cũng xảy ra ở những bệnh nhân được ghép thận.
Ở những bệnh nhân được ghép thận, nồng độ tacrolimus dường như không bị thay đổi bởi CellCept. Tuy nhiên, ở các bệnh nhân ghép gan ổn định, có hiện tượng tăng giá trị AUC của tacrolimus khoảng 20% khi dùng nhiều liều CellCept (1,5g x 2 lần/ngày) phối hợp với tacrolimus.
Các thuốc kháng sinh tiêu diệt các vi khuẩn sản xuất B-glucuronidase trong ruột (ví dụ như aminoglycoside, cephalosporin, fluoroquinolon, và kháng sinh nhóm penicillin) có thể gây ảnh hưởng lên vòng tái tuần hoàn gan ruột MPAG/MPA vì vậy dẫn đến giảm nồng độ MPA (xem mục Cảnh báo và thận trọng, tương tác thuốc)
Thông tin liên quan đến các kháng sinh như sau:
Ciprofloxacin hoặc amoxicillin phối hợp với clavulanic acid: Giảm 54% nồng độ MPA (trũng) trước liều đã được ghi nhận ở bệnh nhân ghép thận vào những ngày ngay sau khi bắt đầu uống ciprofloxacin và amoxicillin phối hợp với clavulanic acid.
Ảnh hưởng này có xu hướng giảm bớt việc tiếp tục sử dụng kháng sinh và hết hẳn khi ngừng sử dụng kháng sinh. Sự thay đổi nồng độ trước liều này có thể không đại diện cho nồng độ MPA toàn phần, do đó sự liên quan về mặt lâm sàng của sự thay đổi này hiện vẫn chưa rõ.
Norfloxacin và metronidazole: Norfloxacin kết hợp với metronidazole làm giảm AUC0-48 của MPA 30% sau khi uống liều đơn CellCept. Không có tác dụng này đối với nồng độ MPA với 1 trong hai kháng sinh trên khi chúng được dùng riêng biệt.
Trimethoprim/sulphamethoxazole: Nồng độ MPA (AUC, Cmax) không bị ảnh hưởng khi kết hợp với trimethoprim/sulfamethoxazole
Các tương tác khác:
Dùng phối hợp probenecid với mycophenolate mofetil ở khi làm tăng diện tích dưới đường cong của MPAG 3 lần. Như vậy, các thuốc khác được biết là được bài tiết qua ống thận có thể cạnh tranh với MPAG và do đó tăng nồng độ huyết tương của MPEG hoặc các thuốc thải qua ống thận.
Dùng phối hợp sevelamer với CellCept ở người trưởng thành và ở bệnh nhi sẽ làm giảm nồng độ đỉnh Cmax của MPA khoảng 30% và làm giảm giá trị AUC0-12 của MPA khoảng 25%. Từ dữ kiện này, người ta đề nghị rằng sau khi đã dùng CellCept 2 tiếng mới nên dùng sevelamer và những thuốc calci có ái lực kết gắn với gốc phosphate tự do khác nhằm giảm thiểu tác động của những thuốc này lên sự hấp thu MPA.
Vaccine sống: Vaccine sống không nên dùng cho bệnh nhân có đáp ứng miễn dịch bị suy giảm. Đáp ứng kháng thể với những vaccine khác có thể bị giảm (xem mục Lưu ý và Thận trọng).
Tương kỵ
CellCept dùng đường tĩnh mạch không tương thích với những dung dịch truyền tĩnh mạch khác, ngoại trừ dung dịch truyền tĩnh mạch Dextrose. Không được trộn lẫn hoặc truyền đồng thời CellCept với các thuốc dùng đường tĩnh mạch khác qua cùng một đường truyền.
Bảo quản
Giữ thuốc trong hộp kín, ngoài tầm với của trẻ em. Bảo quản ở nhiệt độ phòng, nơi khô ráo, tránh ánh sáng trực tiếp.
Mọi thông tin trên đây chỉ mang tính chất tham khảo. Việc sử dụng thuốc phải tuân theo hướng dẫn của bác sĩ chuyên môn.
Câu hỏi thường gặp
Dược lực học là gì?
Dược lực học là nghiên cứu các ảnh hưởng sinh hóa, sinh lý, và phân tử của thuốc trên cơ thể và liên quan đến thụ thể liên kết, hiệu ứng sau thụ thể, và tương tác hóa học. Dược lực học, với dược động học, giúp giải thích mối quan hệ giữa liều và đáp ứng, tức là các tác dụng của thuốc. Đáp ứng dược lý phụ thuộc vào sự liên kết của thuốc với đích tác dụng. Nồng độ thuốc ở vị trí thụ thể ảnh hưởng đến tác dụng của thuốc.
Dược động học là gì?
Dược động học là những tác động của cơ thể đối với thuốc trong suốt quá trình thuốc đi vào, ở trong và đi ra khỏi cơ thể- bao gồm các quá trình hấp thụ, sinh khả dụng, phân bố, chuyển hóa, và thải trừ.
Tác dụng phụ của thuốc là gì? Cách phòng tránh tác dụng phụ của thuốc
Tác dụng phụ là những triệu chứng không mong muốn xảy ra khi chúng ta uống thuốc. Các tác dụng phụ này có thể không nghiêm trọng, chẳng hạn chỉ gây đau đầu hoặc khô miệng. Nhưng cũng có những tác dụng phụ đe dọa tính mạng. Cẩn phòng tránh tác dụng phụ của thuốc như: Thông báo các loại thuốc đang sử dụng với bác sĩ, các bệnh lý nền hiện tại, các tương tác của thuốc đến thực phẩm hằng ngày. Đọc kỹ hướng dẫn sử dụng thuốc và nếu gặp tác dụng phụ cần báo ngay cho bác sĩ.
Sử dụng thuốc đúng cách như thế nào?
Sử dụng thuốc đúng cách là uống thuốc theo chỉ dẫn của dược sĩ, bác sĩ. Ngoài ra không dùng nước quả, nước khoáng hoặc các loại nước ngọt đóng hộp có gas để uống thuốc. Không dùng sữa để uống thuốc vì trong thành phần của sữa có chứa canxi. Không dùng cà phê hay nước chè để uống thuốc. Chỉ nên uống cùng nước lọc.
Các dạng bào chế của thuốc?
Có các dạng bào chế thuốc như
Theo thể chất:- Các dạng thuốc thể rắn (thuốc bột, thuốc viên).
- Các dạng thuốc thể mềm (thuốc cao, thuốc mỡ, gel).
- Các dạng thuốc thể lỏng (dung dịch, hỗn dịch, nhũ dịch, xiro).
Theo đường dùng:
- Các dạng thuốc uống (viên, bột, dung dịch, nhũ dịch, hỗn dịch).
- Các dạng thuốc tiêm (dung dịch, hỗn dịch, nhũ dịch, bột pha tiêm, dịch truyền).
- Các dạng thuốc dùng ngoài (thuốc bôi trên da, thuốc nhỏ lên niêm mạc, thuốc súc miệng).
- Các dạng thuốc đặt vào các hốc tự nhiên trên cơ thể (thuốc đặt hậu môn, thuốc trứng đặt âm đạo...).
Đánh giá sản phẩm (0 đánh giá)
Trung bình
5
Lọc theo:
Nguyễn ThảoDược sĩ
Chào bạn
Dạ sản phẩm có giá 2,650,000 ₫/hộp
Dạ sẽ có tư vấn viên nhà thuốc Long Châu liên hệ theo SĐT bạn đã để lại ạ.
Thân mến!
15/01/2025Trả lời
Hỏi đáp (0 bình luận)
Lọc theo:
- Q
quỳnh
xin giá 1 hộp25 ngày trướcHữu ích
Trả lờiNguyễn Phương LanDược sĩ
Chào Chị Quỳnh,
Hiện tại, sản phẩm có giá 2,535,000 ₫/ Hộp.
Chị có thể gửi yêu cầu Tư vấn ngay trên website hoặc tại ứng dụng Long Châu/ZALO OA Nhà thuốc FPT Long Châu để hưởng ưu đãi miễn phí vận chuyển khi đặt giao tại nhà ạ.
25 ngày trướcHữu ích
Trả lời
- DT
Dr Trí
còn hàng không shop2 tháng trướcHữu ích
Trả lờiNguyễn Thị Hồng NgọcDược sĩ
Chào Anh Trí
Dạ sản phẩm Thuốc Cellcept 250mg Roche dự phòng hiện tượng thải ghép cấp tính đang có hàng ở hầu hết các Nhà thuốc Long Châu trên toàn quốc.
Nhà thuốc thông tin đến Anh ạ.
2 tháng trướcHữu ích
Trả lời
- N
như
cho xin giá 1 hộp2 tháng trướcHữu ích
Trả lờiLê Thị Tuyết NhiDược sĩ
Chào chị Như
Hiện tại, sản phẩm Thuốc Cellcept 250mg Roche có giá 2,535,000đ/ hộp
Chị có thể gửi yêu cầu Tư vấn ngay trên website hoặc tại ứng dụng Long Châu / ZALO OA Nhà thuốc FPT Long Châu để hưởng ưu đãi miễn phí vận chuyển khi đặt giao tại nhà ạ.
2 tháng trướcHữu ích
Trả lời
- KT
Khúc tiệp
Báo giá 1 hộp với bạn ơi?3 tháng trướcHữu ích
Trả lờiĐỗ Diệp MinhDược sĩ
Chào anh Tiệp,
Hiện tại, sản phẩm Thuốc Cellcept 250mg Roche dự phòng hiện tượng thải ghép cấp tính (10 vỉ x 10 viên) có giá 2,535,000 ₫/hộp.
Anh có thể gửi yêu cầu Tư vấn ngay trên website hoặc tại ứng dụng Long Châu/ZALO OA Nhà thuốc FPT Long Châu để hưởng ưu đãi miễn phí vận chuyển khi đặt giao tại nhà ạ
3 tháng trướcHữu ích
Trả lời
- TG
Nguyễn thị giang
Thuốc cellcept 250mg còn không ạ6 tháng trướcHữu ích
Trả lờiNguyễn Thị Thuỳ LinhDược sĩ
Chào bạn Nguyễn Thị Giang,
Dạ sản phẩm còn hàng trên hệ thống Nhà thuốc FPT Long Châu.
Dạ sẽ có tư vấn viên nhà thuốc Long Châu liên hệ theo SĐT bạn đã để lại ạ.
6 tháng trướcHữu ích
Trả lời- G
Giang
báo giá này cho em với !6 tháng trướcHữu ích
Trả lời Nguyễn Mai AnhDược sĩ
Chào bạn Giang,
Hiện tại, sản phẩm có giá 2.550.000đ/ hộp ạ.
Tư vấn viên nhà thuốc Long Châu sẽ sớm liên hệ với bạn qua số điện thoại đã cung cấp để hỗ trợ thêm ạ.
6 tháng trướcHữu ích
Trả lời
:format(webp)/00001755_cellcept_250mg_2305_62cd_large_9c2eed693b.jpg)
:format(webp)/Option_1_2_2d9677e5fd.png)
:format(webp)/Option_1_1_2a84e0cd00.png)

:format(webp)/smalls/Badge_52ad415e46.png)
:format(webp)/00001755_cellcept_250mg_2305_62cd_large_9c2eed693b.jpg)
0936xxxxxx