Dược sĩ Đại học có nhiều năm kinh nghiệm trong việc tư vấn Dược phẩm và hỗ trợ giải đáp thắc mắc về Bệnh học. Hiện đang là giảng viên cho Dược sĩ tại Nhà thuốc Long Châu.
Nghiên cứu xác định RFC4 là tác nhân chính gây ung thư vòm họng
Thu Thủy
26/08/2024
Mặc định
Lớn hơn
Mới đây, một nghiên cứu mới từ Đại học Y Quảng Tây đã làm sáng tỏ vai trò quan trọng của yếu tố sao chép C tiểu đơn vị 4 (RFC4) trong ung thư biểu mô vòm họng (NPC), một loại ung thư phổ biến ở Đông và Đông Nam Á.
Nghiên cứu này không chỉ tập trung vào việc xác định cơ chế bệnh sinh của NPC mà còn mở ra khả năng điều trị mới thông qua việc hiểu rõ ảnh hưởng của RFC4 đối với sự tăng sinh tế bào và mối liên hệ với yếu tố phiên mã HOXA10. Những phát hiện này có thể dẫn đến các phương pháp điều trị hiệu quả hơn cho bệnh nhân NPC và cung cấp những hiểu biết sâu sắc hơn về cơ chế phát triển của ung thư này.
Ung thư vòm họng là gì?
Ung thư vòm họng (Nasopharyngeal Carcinoma – NPC) là một bệnh lý ung thư thuộc nhóm “ung thư đầu và cổ” do sự phát triển của các tế bào vảy tại vòm họng. Bệnh này bao gồm các dạng như ung thư hầu họng (phần giữa của họng), ung thư hạ hầu (phần dưới của họng) và ung thư mũi hầu (phần trên của họng nằm ở sau mũi).
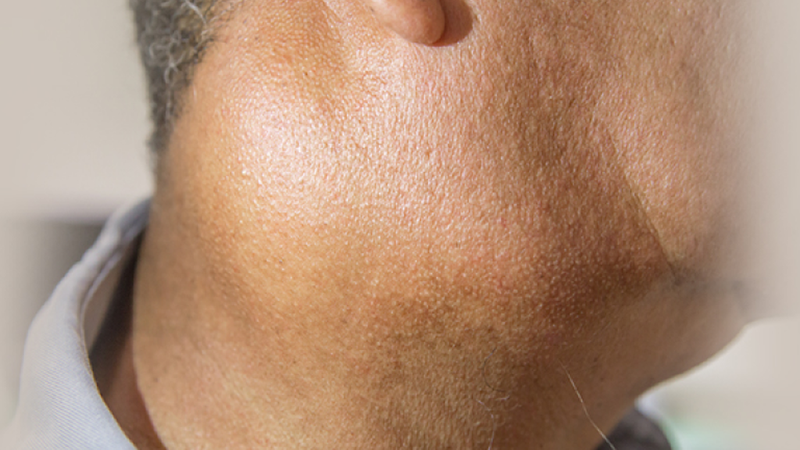
Bệnh ung thư vòm họng thường không có triệu chứng rõ ràng ở giai đoạn đầu. Tuy nhiên, khi tiến triển tại chỗ hoặc đến giai đoạn muộn, bệnh nhân có thể gặp một số triệu chứng như:
- Đau hoặc chảy máu miệng;
- Đau họng, khàn giọng, khó nuốt;
- Ho kéo dài hoặc ho ra máu;
- Đau tai, ù tai hoặc giảm thính lực;
- Nghẹt mũi, chảy máu mũi kéo dài;
- Nhìn mờ, nhìn đôi hoặc bị lé;
- Có khối bướu hoặc hạch ở cổ.
Nguyên nhân, triệu chứng và tiên lượng của ung thư vòm họng có thể khác nhau tùy thuộc vào vị trí và giai đoạn của khối u. Tuy nhiên, điểm chung là hầu hết các trường hợp đều bắt nguồn từ các tế bào vảy biểu mô, loại tế bào mỏng, phẳng giống như vảy cá.
Nghiên cứu về vai trò của RFC4 trong ung thư biểu mô vòm họng
Lichuan Wu và nhóm nghiên cứu tại Đại học Y Quảng Tây (Trung Quốc) đã cùng nhau thực hiện một nghiên cứu toàn diện về vai trò của yếu tố sao chép C tiểu đơn vị 4 (RFC4) trong ung thư biểu mô vòm họng (NPC). Đây là một loại ung thư phổ biến liên quan đến nhiễm trùng virus Epstein-Barr. Nghiên cứu được thực hiện với mục đích tìm hiểu cơ chế bệnh sinh của NPC và xác định các mục tiêu điều trị tiềm năng.
NPC là một loại ung thư phổ biến ở khu vực Đông và Đông Nam Á, với hơn 133.000 trường hợp mới được chẩn đoán vào năm 2020 theo Cơ quan Nghiên cứu Ung thư Quốc tế (IARC). Các phương pháp điều trị chính cho NPC bao gồm xạ trị, hóa xạ trị đồng thời và liệu pháp miễn dịch. Mặc dù tỷ lệ sống sót sau 5 năm đã được cải thiện, nhưng vẫn còn nhiều lo ngại về các bệnh dai dẳng và tái phát. Các protein thuộc họ yếu tố sao chép C (RFC), bao gồm RFC4, đóng vai trò quan trọng trong quá trình sao chép và sửa chữa DNA. Nghiên cứu đưa ra giả thuyết rằng RFC4 có thể đóng vai trò quan trọng trong NPC, một giả thuyết chưa được nghiên cứu sâu trước đây.
Cơ chế bệnh sinh của NPC qua yếu tố RFC4 và HOXA10
Nghiên cứu áp dụng nhiều phương pháp khác nhau như phân tích tin sinh học, nuôi cấy tế bào, xét nghiệm chuyển nhiễm, xét nghiệm hình thành nhân bản đĩa, phát hiện chu kỳ tế bào, chiết RNA và qPCR thời gian thực, giải trình tự RNA, Western blot và mô hình xenograft chuột. Phân tích thống kê cũng được thực hiện để đo lường mối tương quan giữa RFC4 và các gen khác cũng như so sánh các nhóm thử nghiệm khác nhau.
Kết quả nghiên cứu chỉ ra rằng, RFC4 là một gen chủ chốt có khả năng liên quan đến nguyên nhân khối u NPC thông qua phân tích tin sinh học, bao gồm phân tích mạng lưới biểu hiện gen đồng trọng số (WGCNA). Biểu hiện của RFC4 được phát hiện là cao hơn ở các mô khối u NPC so với mô bình thường, điều này được xác nhận bằng xét nghiệm hóa mô miễn dịch (IHC). Việc phân hủy RFC4 trong tế bào NPC dẫn đến ức chế sự tăng sinh tế bào và hình thành dòng vô tính trong ống nghiệm, đồng thời gây ra sự dừng chu kỳ tế bào ở pha G2/M. Nghiên cứu cũng phát hiện rằng RFC4 điều chỉnh sự biểu hiện của yếu tố phiên mã homeobox HOXA10, yếu tố liên quan đến sự biệt hóa và hình thành tế bào cũng như liên quan đến nhiều loại ung thư khác.
Những phát hiện này cho thấy RFC4 có thể đóng vai trò quan trọng trong sự phát triển của NPC và cơ chế thúc đẩy tăng sinh tế bào của nó có thể khác biệt so với các loại ung thư khác. Nghiên cứu cũng chỉ ra rằng HOXA10 là một mục tiêu tiềm năng của RFC4, và sự biểu hiện quá mức của HOXA10 có thể đảo ngược một phần tác dụng ức chế của việc làm im lặng RFC4 đối với sự tăng sinh tế bào NPC. Điều này gợi ý rằng RFC4 có thể thúc đẩy sự tăng sinh tế bào NPC thông qua việc điều chỉnh HOXA10.
Nghiên cứu này đóng góp quan trọng vào việc hiểu biết về sinh bệnh học của NPC và mở ra khả năng điều trị mới. Những phát hiện này mở đường cho các nghiên cứu tiếp theo về cơ chế mà RFC4 điều chỉnh biểu hiện HOXA10 và ý nghĩa của nó trong việc điều trị NPC.
Các bài viết liên quan
Long Châu đồng hành cùng Tập đoàn IHH Singapore với buổi gặp gỡ chuyên gia từ Singapore với thông điệp "Phòng bệnh, chăm sóc và điều trị ung thư"
Tế bào ung thư là gì? Cơ chế hình thành và phát triển tế bào ung thư
Chụp CT có phát hiện ung thư dạ dày không? Các xét nghiệm khác để chẩn đoán ung thư dạ dày
Vi khuẩn ăn khối u ung thư đã ra đời, mở ra hướng điều trị mới
Ung thư nào chết nhanh nhất và vì sao diễn tiến lại nguy hiểm?
Ung thư di căn có chữa được không? Phương pháp điều trị ung thư di căn
Khám tầm soát ung thư là gì? Ai nên thực hiện?
Đề xuất bổ sung nhiều thuốc vào danh mục chi trả bảo hiểm y tế, trong đó có 30 thuốc điều trị ung thư
Gừng ngâm mật ong chữa ung thư có đúng không?
Ung thư có lây không? Giải đáp khoa học
:format(webp)/Option_1_2_2d9677e5fd.png)
:format(webp)/Option_1_1_2a84e0cd00.png)
:format(webp)/ds_my_huyen_780f9bef46.png)